2019
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6359194/
Drug Bioavailability Enhancing Agents of Natural Origin (Bioenhancers) that Modulate Drug Membrane Permeation and Pre-Systemic M
Many new chemical entities are discovered with high therapeutic potential, however, many of these compounds exhibit unfavorable pharmacokinetic properties due to poor solubility and/or poor membrane permeation characteristics. The latter is mainly due ...
www.ncbi.nlm.nih.gov
Drug Bioavailability Enhancing Agents of Natural Origin (Bioenhancers) that Modulate Drug Membrane Permeation and Pre-Systemic Metabolism
경구 투여 경로
그림 3는 경구 투여 경로를 통한 개선된 약물 전달을 위한 선택된 바이오 인핸서의 주요 작용 기전을 설명합니다.
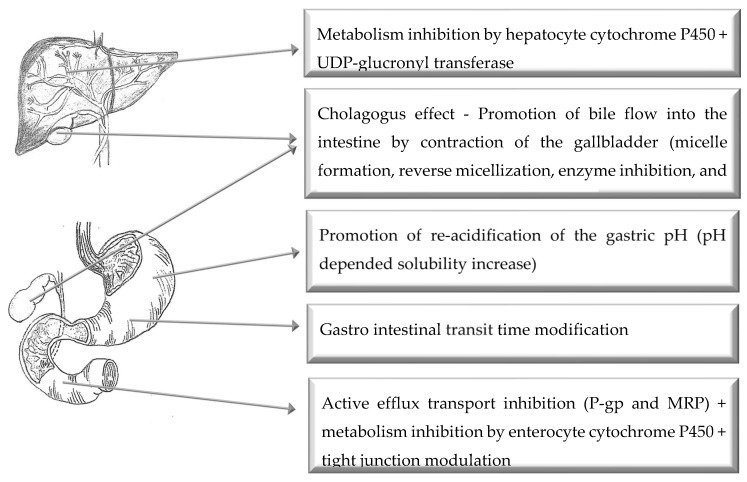
향상된 경구 약물 전달을 위한 생체 인핸서의 주요 작용 메커니즘의 그림.
4.1. 알로에 베라
4.2.Bile Salts
4.3. 블랙 커 민
일반적으로 블랙 커민/캐러웨이로 알려진 Nigella sativa 는 이전에 아목시실린의 생체 강화제로 평가되었습니다
N. sativa의 이러한 투과 향상 효과는 지방산의 존재에 기인할 수 있다고 제안되었습니다
지방산은 정점과 기저외측막의 유동성을 증가시켜 투과성이 낮은 약물의 투과를 향상시킬 수 있다는 것이 이전에 입증되었습니다..
토끼에 대해 수행된 유사한 생체 내 연구에서 반대 결과가 나타났습니다. 그 연구에서, 사이클로스포린(30 mg/kg)의 C max 및 AUC 0-∞ 는 Nigella (200 mg/kg) 로 전처리한 후 각각 35.5% 및 55.9%로 유의하게 감소했습니다 .
그러나 사이클로스포린 청소율의 상당한 증가(~2배)가 관찰되었으며, 이는 장내 P-gp 및/또는 CYP3A4가 N. sativa 의 존재하에 활성화됨을 시사합니다.
4.4. 캡사이신
캡사이신이 있는 상태에서 펙소페나딘을 capsaicin 전처리와 표준 P-gp 억제제인 verapamil로 얻은 결과가 비슷했기 때문에 쥐의 장에서 P-gp 유출 억제가 작용 기전으로 제시되었다
결과는 캡사이신이 P-gp 매개 약물 유출의 억제를 통해 펙소페나딘의 생체 이용률을 증가시킬 수 있다는 생체 내 증거를 제공합니다.
4.5. Caraway
Caraway는 Carum carvi 라는 식물의 잘 익은 말린 과일에서 얻습니다 .
Cmax 의 증가 는 rifampicin, isoniazid 및 pyrazinamide에 대해 각각 32.22%, 36.01% 및 33.22%였으며, AUC 0-24 h의 증가 는리팜피신, 이소니아지드 및 피라진아미드의 경우 각각 32.16%, 29.06% 및 27.92%였습니다.
저자에 따르면 Caraway 추출물에 의한 생체 이용률의 향상은 P-gp 유출에 대한 영향뿐만 아니라 점막에서 장막 투과의 향상에 기인할 수 있습니다.
Caraway는 P-gp 유출의 억제제로 작용하는 것으로 나타났으며 주요 활성 성분은 carvone과 limonene인 것으로 밝혀졌습니다.
4.6. Cyclosporine A
Cyclosporine A는 11개의 아미노산으로 구성된 폴리펩티드이며 처음에는 곰팡이인 Tolypocladium inflatum Gams 에서 파생되었습니다
Cyclosporine A는 유출 수송체 P-gp의 억제제로 작용하는 것으로 나타났으며 결과적으로 이 활성 유출 수송체의 기질인 약물의 생체 이용률을 증가시킬 수 있습니다.
10 mg/kg의 사이클로스포린 A 와 30 mg/kg의 클로피도그렐을 병용 투여했을 때 클로피도그렐의 AUC와 Cmax가 각각 3.48배 및 2.83배 증가 했습니다 . .
저자는 이러한 생체이용률 증가가 P-gp 매개 유출의 억제에 기인한다고 밝혔습니다.
4.7. 키토산 및 유도체
약물 흡수 향상의 주요 메커니즘은 친수성 및 거대분자 약물 화합물의 세포주위 흡수를 향상시키기 위한 긴밀한 접합 조절을 포함하는 것으로 나타났습니다.
4.8. 커큐민
커큐미노이드와 기존 약물의 약동학적 상호작용에 대한 이전에 발표된 리뷰에서는 CYP450 및 II상 효소의 조절, P-gp 유출 억제 및 OATP(유기 음이온 수송 폴리펩타이드)에 대한 잠재적 효과를 통한 잠재적 상호작용이 밝혀졌습니다.
불행히도, 약물 흡수 증진에서 커큐민에 의한 약물 흡수 감소에 이르기까지 다양한 연구에 의해 대조적인 결과가 얻어졌습니다.
Western blot 분석 결과 장내 P-gp 단백질 발현이 49% 감소한 것으로 나타났습니다. CYP3A 단백질 함량은 커큐민 전처리 4일 후 42% 감소했습니다.
반면, 간 P-gp 단백질 발현은 144% 증가하였고 CYP3A 단백질 함량은 91% 증가하였다.
신장 P-gp 단백질 수준은 변하지 않았지만 신장 CYP3A는 41% 향상되었습니다.
celiprolol은 P-gp 기질이고 midazolam은 CYP3A 효소에 의해 광범위하게 대사되기 때문에 이 연구에서 이 두 약물의 약동학은 소장에서 P-gp와 CYP3A의 하향 조절로 인해 커큐민에 의해 변화되었음을 추론했습니다.
4.9. 디오스민
감귤류 과일의 특정 플라본(예: tangeretin, nobiletin 및 bergamottin)은 P-gp 억제 효과를 나타내어 이 유출 수송체의 기질인 약물과 약동학적 상호작용을 일으켰습니다.
연구 결과에 따르면 diosmin은 P-gp 유출 수송 억제제로 작용하여 P-gp의 기질인 약물의 생체 이용률을 향상시킬 수 있는 가능성이 있음이 분명합니다
4.10. 에모딘
에모딘(1,3,8-트리하이드록시-6-메틸-안트라퀴논)과 같은 안트라퀴논은 Rheum palmatum [ 163 ], Polygonum multiflorum [ 164 ], Polygonum cuspidatum [ 165 ], Cassia 와 같은 다양한 식물과 허브에서 자연적으로 발생합니다 .
emodin이 P-gp의 효과적인 억제제이며 그 효과가 P-gp에 대한 직접 결합 및 후속적인 P-gp 매개 유출 기능의 약화 또는 P-gp 표현 감소와 관련된 간접적 기전에 의해 매개됨을 확인했습니다.
저자는 emodin이 P-gp 관련 유출의 유도제이자 MRP3의 억제제라고 결론지었습니다.
4.11. Gallic Acid Ester
갈산은 P-gp 매개 약물 유출과 CYP3A4와 같은 CYP450 관련 동위효소에 대한 억제 효과를 나타내는 것으로 보고되었습니다
시험관 내 연구 결과에 따르면 딜티아젬의 겉보기 투과성은 갈산 존재 시 십이지장, 공장 및 회장의 비외향성 장낭의 각 부분에서 4.4배, 5.1배 및 4.9배 증가했습니다. 대조군과 비교할 때
갈산은 P-gp와 CYP3A4의 이중 억제제일 가능성이 가장 높으며 이러한 이중 효과가 딜티아젬의 생체 이용률을 크게 향상시킬 수 있음을 시사했습니다
연구 시작 전 7일 동안 쥐에게 갈산(50mg/kg)을 사전 처리했습니다. metoprolol의 C max 및 AUC 값의 상당한 증가 가 분명했습니다.
갈산은 간에서 CYP2D6 활성을 억제하여 경구 생체이용률을 향상시켜 metoprolol의 대사를 감소시키는 것으로 결론지었습니다.
4.12. 제니스테인
제니스테인은 그 자체로 생체이용률이 매우 낮고 일부 연구에서는 제니스테인이 항암 효과가 있을 수 있다고 제안했지만 낮은 생체이용률 때문에 임상 연구에서는 이러한 효과를 얻을 수 없었습니다[ 183].
Genistein은 P-gp, BCRP 및 MRP2 수송체의 유출을 억제하는 것으로 나타났기 때문에 약물의 생체이용률 향상제로 알려져 있습니다.
33μM 제니스테인에 대해서는 수송 억제를 측정할 수 없었지만 100μM 제니스테인에서는 20% 억제가 나타났습니다.
제니스테인이 P-gp를 억제하지만 P-gp의 기질로 보이지는 않는다는 것이 이후에 결정되었습니다.
그러나, 제니스테인에 노출된 후 P-gp 발현의 상관 변화는 관찰되지 않았으며, 이는 P-gp 활성만 조절되었음을 나타냅니다.
Genistein은 또한 인간 적혈구에서 MRP1 기질인 2',7'-비스-(카르복시프로필)-5(6)-카르복시플루오레세인(BCPCF)의 유출을 억제했습니다.
Genistein 은 BCPCF 유출에 대해 50-70μM 의 IC 50 농도를 표시했습니다.
제니스테인은 MRP1 유출 수송체를 억제하지만 이 조절은 기질에 민감한 것으로 보고되었습니다.
제니스테인은 보다 최근의 연구에서 (-)-에피갈로카테킨-3-갈레이트(EGCG)의 생체 변형 및 장 유출을 억제하는 것으로 나타났습니다.
HT-29 인간 결장암 세포에서 제니스테인(20μM)이 있을 때 세포질 EGCG가 2~5배 증가하는 것을 보여주었습니다.
그들은 또한 200mg/kg 제니스테인과 75mg/kg EGCG로 CF-1 마우스를 처리하여 혈장 반감기와 EGCG의 최대 농도를 증가시켰습니다.
그러나 수컷 선종성 대장균(APC) min/+ 마우스 모델에서 이 조합은 또한 종양 발생을 향상시켰습니다.
주목해야 할 중요한 것은 Chen 등의 연구 결과입니다. [ 189 ],
이는 제니스테인이 2상 약물 대사 효소인 설포트랜스퍼라제를 유도할 수 있음을 나타냅니다.
효소 활성, 단백질 수준 및 mRNA 발현은 형질전환된 인간 간 세포주(HepG2) 및 결장암 세포주(Caco-2)에서 평가되었습니다.
유전자 발현(SULT1A1 및 SULT2A1)은 시간 및 용량 의존적(0-25μM) 방식으로 제니스테인에 의해 유도된다는 결론을 내렸습니다.
대조적으로, 약 0.1μM의 제니스테인은 인간의 간 페놀 설포트랜스퍼라제를 경쟁적인 방식으로 50% 억제했습니다[ 190 ].
4.13. Gokhru 추출물
Ayurvedic 의약품에 사용되는 인기 있는 식물 추출물인 Gokhru 추출물은 Tribulus terrestris Linn(Zygophyllaceae)에서 파생됩니다
Gokhru 추출물은 전통적으로 이뇨제, 항염증제, 동화 작용, 경련 완화제, 근육 이완제, 혈압 강하제 및 혈당 강하제로 사용되지만 병용 투여되는 약물의 생체 이용률에 영향을 미치는 것으로 보고되었습니다.
메트포르민은 용해도가 높지만 막 투과성이 낮은 것으로 알려진 항당뇨병 약물(BCS class III)입니다.
결과는 Gokhru 추출물이 있을 때 메트포르민의 흡수가 증가하는 것으로 나타났으며 저자는 추출물의 주요 사포닌 성분이 약물 수송의 이러한 증가에 크게 기여했을 수 있다고 제안했습니다.
사포닌은 스테로이드 또는 트리테르페노이드 아글리콘에 연결된 하나 이상의 당 사슬로 구성됩니다.
그것은 세포막 구조의 대부분을 유지하면서 콜레스테롤을 가용화할 수 있어 세포막을 투과시켜 막 투과성을 증가시킵니다
.
4.14. 자몽 주스
자몽( Citrus paradisi ) 주스와 칼슘 채널 길항제인 펠로디핀 사이의 약동학적 상호 작용은 에탄올과 펠로디핀 간의 잠재적 상호작용을 평가하기 위해 설계된 1989년 생체 내 임상 연구에서 우연히 발견되었습니다.
자몽 주스와 함께 펠로디핀을 섭취하면 항고혈압 효과와 펠로디핀 혈장 농도가 높아집니다.
이 관찰은 펠로디핀 혈장 농도가 물보다 자몽 주스와 함께 섭취했을 때 5배 이상 높은 것으로 밝혀진 단일 지원자에 대한 후속 파일럿 연구로 이어졌습니다.
이 초기 발견 이후 85개 이상의 약물이 약동학 측면에서 자몽 주스와 상호 작용하는 것으로 나타났으며 이 중 가장 많이 경험한 것은 혈장 농도 증가입니다[ 193 ].
이 효과는 자몽 주스와 함께 펠로디핀을 정맥 투여한 경우 관찰되지 않았으며, 이는 CYP3A4와 관련된 전신 대사의 선택적 억제를 나타냅니다.
여러 연구에 따르면 자몽 주스가 약물의 약동학적 매개변수에 미치는 영향과 관련하여 세 그룹, 즉 "증가", "감소" 및 "변화 없음"이 구별될 수 있음이 나타났습니다.
여러 연구의 결과에 따르면 시간이 지남에 따라 여러 형태의 자몽(즉, 전체 과일, 신선한 과일 주스 또는 냉동 농축액)의 약동학적 효과가 약물 특이적이며 어떤 경우에는 농도 의존적일 수 있습니다.
또한 전신 대사로 인해 약물의 고유한 생체 이용률이 낮을수록 자몽과의 상호 작용이 위험할 수 있는 가능성이 더 높은 것으로 나타났습니다.
약물(예: 펠로디핀)의 생체 이용률을 증가시키는 자몽 주스의 주요 작용 기작 중 하나는 소장의 장세포와 간의 간세포에서 CYP3A4의 기전 기반 억제에 의한 것입니다.
또한 자몽 주스가 P-gp 유출 수송체를 억제하여 이 유출 수송체(예: 탈리놀롤)의 기질인 약물의 생체 이용률을 증가시킬 수 있는 것으로 나타났습니다
한편, 자몽 주스는 OATP, 특히 OATP1A2 및 OATP2B1과 같은 흡수 수송체를 억제하는 능력이 있어 특정 약물(예: 펙소페나딘)의 흡수를 감소시킬 수 있음이 밝혀졌습니다[.
4.15. 리코펜
심바스타틴을 함유한 리코펜 함유 나노 제제가 저밀도 지단백(LDL)에 미치는 영향이 경미한 고콜레스테롤혈증 환자에서 조사되었습니다.
이 연구의 목적은 심바스타틴의 간 생체이용률을 특이적으로 향상시키기 위한 간내 수송의 벡터로서 라이코펜을 평가하는 것이었습니다.
리코펜의 작용 메커니즘은 이중 카로티노이드/LDL 수용체 매개 메커니즘을 통해 간 흡수를 향상시킵니다
Lyco-Simvastatin의 약리학과 관련된 추가 연구가 필요하지만 lycopene은 simvastatin의 표적 간 전달을 위한 유망한 바이오 인핸서인 것으로 보입니다.
4.16. Lysergol
리세르골(9,10-디데하이드로-6-메틸에르골린-8- O- 메탄올)은 여러 고등 식물(예: Ipomoea violacea , I. muricata 및 Rivea corymbosa ) 및 하등 균류(예: Claviceps , Penicillium 및 Rhizopus )에 존재하는 화합물입니다 .
Lysergol은 전통적으로 향정신성, 진통제, 진통제, 저혈압 및 면역 자극제로 사용됩니다.
일반적으로 혈관 활동을 통해 정상적인 혈류를 유지하고 위장관에서 약물 흡수를 촉진할 수 있습니다.
lysergol은 생체 이용률을 증가시키고 curcumin의 제거를 유의하게 감소시켰습니다. .
P-gp보다는 BCRP가 lysergol에 의해 억제되었음을 시사했습니다.
P-gp 기질인 디곡신(digoxin)과 BCRP 기질인 설파살라진(sulfasalazine)에 대한 현장 단일 통과 장 관류 연구는 20mg/kg 리세르골로 전처리한 후 Sprague-Dawley 쥐에서 수행되었습니다.
이러한 연구는 P-gp가 lysergol의 투과 증진 효과에 관여하지 않고 BCRP가 억제된다는 결론을 뒷받침합니다[ 62 ].
리세르골에 의해 리팜피신과 테트라사이클린 장내 수송이 향상될 수 있음을 보여주었습니다.
Lysergol은 또한 수컷 Sprague-Dawley 쥐에서 4급 프로토베르베린 알칼로이드인 베르베린의 경구 생체이용률을 증가시켰습니다.
베르베린은 세균 감염, 장내 기생충 감염 및 설사를 포함한 수많은 질병에 사용되지만 장에서 매우 잘 흡수되지 않고 광범위하게 대사됩니다.
이 연구는 20 mg/kg lysergol이 베르베린의 생체이용률을 증가시킬 수 있음을 나타냈습니다[ 61 ].
4.17. 나린진과 베르가모틴
자몽에 함유된 나린진(플라보노이드) 및 베르가모틴(푸라노쿠마린)과 같은 특정 식물 화학 물질은 특정 약물과 함께 투여된 자몽 주스에서 관찰되는 약동학적 상호작용과 관련이 있습니다.
paclitaxel이 Sprague-Dawley 쥐에게 naringin과 함께 경구 투여되었을 때, paclitaxel 혈장 농도는 통계적으로 유의하게 증가했습니다.
naringin은 CYP3A 및 P-gp의 알려진 억제제인 quercetin과 유사하게 paclitaxel의 생체이용률에 영향을 미치므로 naringin은 CYP3A 대사 및 P-gp 유출 수송체의 억제를 통해 paclitaxel의 생체이용률을 향상시킨 것으로 추론됩니다.
naringin이 diltiazem의 대사를 억제하는 능력을 확인시켜주었습니다[ 64 ].
베르가모틴은 기질 의존적 가역적 억제제이지만 CYP3A4의 기질 비의존적 기전 기반 억제제로 확인되었습니다.
한편, 6',7'-dihydroxybergamottin은 기질에 의존하지 않는 가역적이고 메커니즘 기반의 CYP3A4 억제제인 것으로 밝혀졌습니다.
4.18. 팔미토일 카르니틴 클로라이드
4.19. 피페린
피페린은 후추( Piper nigrum )와 롱페퍼( Piper longum )[ 11 ]에 함유된 알칼로이드입니다.
피페린은 전통적으로 항염증, 해열, 항진균, 설사 및 항암 효과로 사용됩니다.
피페린이 생체 강화 효과를 일으키는 가능한 메커니즘에는 막 역학의 변경, P-gp 유출 억제, 위장 및 간 대사 억제가 포함됩니다.
C57BL 마우스에 경구 투여했을 때 피페린이 레스베라트롤(3,5,4'-트리하이드록시스틸벤)의 혈청 수준에 미치는 영향을 조사한 연구에서 AUC와 Cmax 가 각각 229% 및 1,544% 증가하는 것으로 나타났습니다.
피페린의 효과는 정맥 투여(간 대사 억제로 인해)보다 경구 투여(위장관 상피에서 P-gp 매개 유출 억제 및 대사 억제로 인해) 후에 더 현저한 것으로 추론되었습니다 .
4.20. 케르세틴
CYP3A4 및 P-gp 억제제인 케르세틴은 쥐에서 경구 투여된 타목시펜과 4-하이드록시타목시펜의 생체 이용률을 유의하게 향상시키는 능력을 보여주었습니다
타목시펜의 상대 생체이용률은 1.35배 및 1.61배 더 높았으며 절대 생체이용률은 2.5 및 7.5mg/kg 케르세틴에서 각각 20.2% 및 24.1%였습니다. .
흥미롭게도 더 높은 농도의 케르세틴(15mg/kg)은 유의한 변화를 유도하지 않았습니다. .
이러한 결과는 타목시펜의 MDR 유출 및 초회 통과 대사가 케르세틴에 의해 억제됨을 시사한다.
또 다른 생체 내 연구에서 펙소페나딘이 케르세틴과 함께 투여되었을 때 P-gp 유출에 대한 억제 효과가 입증되었습니다
요약하면, 케르세틴은 장 흡수를 향상시키고 따라서 타목시펜 과 펙소페나딘의 생체이용률을 높이기 위한 생체 증강제로 사용될 수 있습니다.
케르세틴이 사용하는 작용 메커니즘은 MDR 수송체 유출 억제와 초회 통과 대사 억제입니다[ 95 ]. .
펙소페나딘의 P-gp 매개 유출에 대한 퀘르세틴의 억제 효과가 단기(7일)에 입증되었지만, 퀘르세틴을 장기간 사용하여 동일한 결과를 얻을 수 있는지 여부는 불확실합니다.
4.21. 퀴니딘
장에서 paeoniflorin의 흡수는 quinidine의 동시 투여에 의해 크게 향상될 수 있습니다.
4.22. 레스베라트롤
최근 연구에서는 레스베라트롤이 생체 내 및 시험관 내에서 쥐의 장내 메토트렉세이트 흡수를 유의하게 증가시킬 수 있음을 보여주었습니다
레스베라트롤이 P-gp 또는 MRP2를 억제함으로써 메토트렉세이트 장 흡수를 향상시킬 수 있음을 시사합니다.
또한, 메토트렉세이트와 레스베라트롤의 병용 투여는 메토트렉세이트의 누적 요배설량을 37.3% 감소시켰으며, 이는 레스베라트롤이 메토트렉세이트의 신장 배설을 억제할 수 있음을 나타냅니다.
생체 내 및 시험관 내 결과는 레스베라트롤이 장에서 메토트렉세이트의 흡수를 유의하게 증가시킬 수 있고 또한 메토트렉세이트 신장 청소율을 감소시킬 수 있음을 나타냅니다.
4.23. Sinomenine
4.24. Sodium caprate(지방산)
베르베린 처리군과 비교하여 카프르산나트륨을 함유한 베르베린은 혈당 수치와 혈당 곡선 아래 면적을 현저히 감소시켜 인슐린의 항당뇨 활성을 향상시켰다.베르베린의 낮은 생체이용률은 P-gp 유출로 인한 것으로 제안됩니다.
소듐 카프레이트가 P-gp 유출을 억제할 수 있다는 것이 이전에 입증되었습니다.
4.25. Zonula Occludens 독소 (Zot)
'약물' 카테고리의 다른 글
| 실리마린, 커큐민, 녹차 및 포도씨 추출물과 같은 식물성 폴리페놀의 파이토솜 복합체의 생체이용률 및 활성 (0) | 2022.11.25 |
|---|---|
| 베툴린 및 베툴린산 (0) | 2022.11.25 |
| CYP3A4 (0) | 2022.11.08 |
| Apigenin (0) | 2022.11.05 |
| 메벤다졸 (0) | 2022.11.04 |