https://www.mdpi.com/1422-0067/20/8/2025/htm
<Pharmacological Applications of Nrf2 Inhibitors as Potential Antineoplastic Drugs>
2019
Pharmacological Applications of Nrf2 Inhibitors as Potential Antineoplastic Drugs
Oxidative stress (OS) is associated with many diseases ranging from cancer to neurodegenerative disorders. Nuclear factor-erythroid 2 p45-related factor 2 (Nrf2) is one of the most effective cytoprotective controller against OS. Modulation of Nrf2 pathway
www.mdpi.com
(Nrf2)는 OS에 대한 가장 효과적인 세포 보호 조절제 중 하나입니다. Nrf2 경로의 조절은 항종양 치료에서 놀라운 전략을 구성합니다.
Nrf2의 활성화가 다양한 암에서 발생함에도 불구하고 많은 수의 Nrf2-항산화 반응 요소 활성화제가 암과 같은 OS 관련 질병에서 화학 예방 약물로 사용하기 위해 스크리닝되었습니다.
연구에 따르면 Nrf2 경로의 과활성화는 정상 세포와 악성 세포의 생존을 돕는 상황을 만들어 OS, 항암제 및 방사선 요법으로부터 보호합니다.
발암 과정에서 정상 세포는 종양 세포로 진화하며, 이는 개시, 촉진 및 진행의 3단계로 여러 후성 유전적 및 유전적 사건을 포함하는 다단계 과정입니다[ 2].
암 치료에는 여러 가지 유형이 있습니다. 환자가 받게 될 치료 유형은 암의 유형과 진행 정도에 따라 다릅니다. 오늘은 암을 치료하기 위한 수술, 방사선 요법, 화학 요법, 면역 요법, 표적 요법, 호르몬 요법 및 줄기 세포 이식 과정에 대해 이야기할 수 있습니다. 또한 정밀 의학은 의사가 환자의 질병에 대한 유전적 이해를 바탕으로 환자에게 가장 도움이 되는 치료법을 선택하도록 돕습니다.
OS는 세포 운명을 결정하는 데 중요한 역할을 합니다.
과도한 활성산소(ROS) 부하에 대한 반응으로 세포자멸사 신호 전달 경로가 자극되어 정상적인 세포 사멸을 촉진합니다.
핵 인자-적혈구 2 p45 관련 인자 2(Nrf2)는 세포를 방어하는 주요 조절자처럼 보입니다[ 12 ].
Nrf2는 일반적으로 Keap1 억제제와의 상호작용에 의해 세포질에서 분해됩니다.
그러나 과도한 양의 ROS는 티로신 키나아제를 자극하여 Nrf2를 분리합니다.
돌연변이 및 자극된 업스트림 종양유전자로 인한 Nrf2 및/또는 Keap1의 탈조절은 세포자멸사로부터 세포를 보호하고 증식, 전이 및 화학저항성을 유도하기 위한 Nrf2의 핵 축적 및 활성화와 관련이 있습니다.
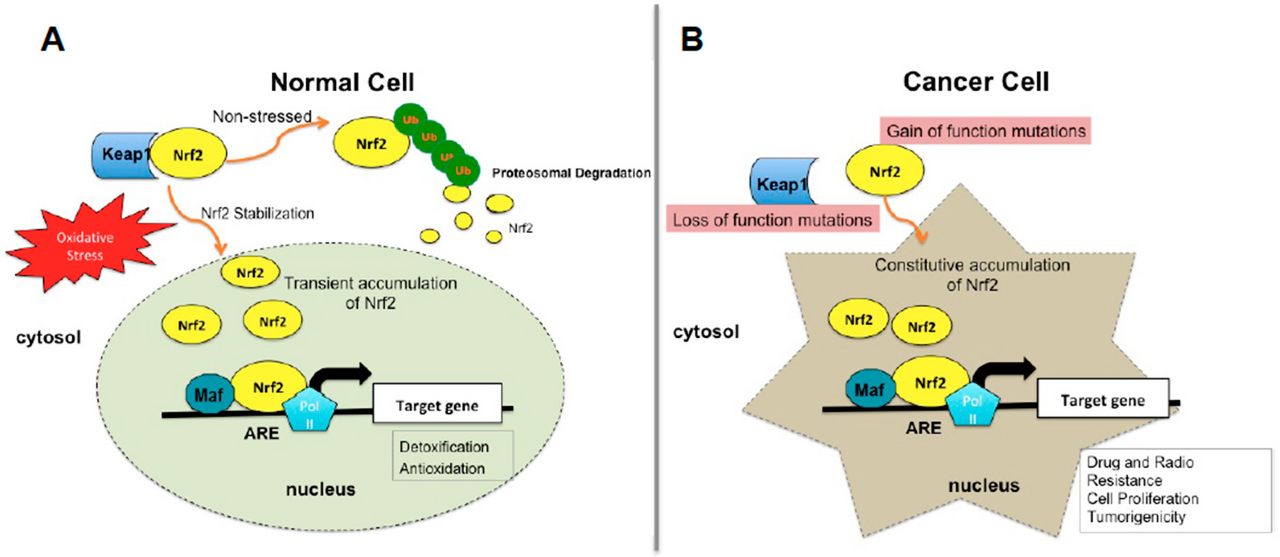
그림 1. 정상 세포와 암세포의 Nrf2 상태.
( A ) 정상 세포에서 정상 조건에서 Keap1은 유비퀴틴화 및 프로테아좀 분해를 통해 Nrf2의 전사 활성을 억제하고 스트레스 조건에서는 Keap1과 Nrf2 상호 작용이 발생하지 않아 Nrf2 안정화 및 핵 축적을 유발하여 세포 보호 유전자 발현을 유도합니다.
( B) 암세포에서 NRF2(기능 돌연변이 획득) 및 KEAP1(기능 상실 돌연변이)의 체세포 돌연변이는 Nrf2의 구성적 활성화를 초래하여 종양 형성과 관련된 유전자의 발현을 유도합니다.
Nrf2, 핵 인자 적혈구계 2-관련 인자 2; Keap1, Kelch-유사 ECH-연관 단백질 1; Maf, 작은 근건막성 섬유육종 단백질; 폴 II; 폴리머라제 II; ARE: 항산화 반응 요소
잠재적인 항종양 약물로서의 Nrf2 억제제
일부 Nrf2 억제제는 Nrf2 중독 암의 치료를 위해 언급되었습니다.
그 중 하나는 천연 쿼시노이드인 브루사톨입니다. 브루사톨은 Nrf2의 폴리유비퀴틴화를 자극하여 Nrf2 단백질 수준을 감소시키는 것으로 밝혀졌습니다.
Nrf2에 대한 brusatol의 억제 효과는 억제인자 Keap1에 의존하지 않는 것으로 밝혀졌습니다.
Brusatol은 Nrf2 신호 전달의 억제에 유익한 것으로 밝혀졌습니다[ 102 ].
루테올린은 항산화 반응 요소 주도 유전자 발현의 억제제로 밝혀졌습니다.
또 다른 Nrf2 억제제인 할로푸지논(halofuginone)은 Nrf2에 중독된 암 세포에 대한 화학 민감성 영향을 개발하기 위해 확립되었습니다[ 106 ].
Bardoxolone methyl(BM)은 천연 제품인 올레아놀산과 유사하며 반합성 트리테르페노이드는 Nrf2를 효과적으로 유도하며 백혈병 및 일부 고형 종양과 같은 다양한 유형의 암에서 조사되었습니다[ 108 , 109 ].
BM은 Michael 수용체 활성을 나타내며 Nrf2의 가장 강력한 유도자로 작용합니다[ 110 ].
Camptothecin은 Nrf2를 많이 발현하는 암을 치료하는 효과를 향상시키기 위해 다른 항암제와 함께 제안될 수 있는 또 다른 새로운 Nrf2 억제제입니다.
Camptothecin은 HepG2, SMMC-7721 및 A549를 비롯한 다양한 유형의 암 세포주에서 Nrf2 발현 및 전사 작용을 분명히 억제하는 것으로 밝혀졌습니다[ 111 ].
Nrf2는 거의 모든 세포 유형과 조직에서 발견되지만 장, 폐, 신장과 같이 주요 해독 반응이 일어나는 조직에서 두드러집니다.
그것은 ARE에 결합을 통해 산화적 손상과 발암에 대한 보호 역할을 합니다[ 115 ].
최근 연구에 따르면 Nrf2를 표적으로 하는 것은 종양을 줄이고 방어력을 개발하는 새로운 치료법이 될 수 있습니다.
Nrf2가 OS에서 정상 세포를 방어하고 있음이 확인되었습니다.
종양 세포의 과잉 Nrf2는 세포 보호에 대한 방어를 계속합니다.
이것은 OS에 대해 종양 세포를 방어하는 데 도움이 될 수 있습니다.
암세포가 증가된 OS에서 생존하고 치료에 저항하기 위해 스스로를 조정하는 이 과정을 "산화환원 적응"이라고 합니다.
따라서 Nrf2의 활성화 또는 억제가 암의 예방 또는 치료에 유익한지 여부는 논란의 여지가 있습니다[ 116 ].
수많은 화합물이 Nrf2 경로를 조절하여 항암 활성을 수행합니다.
Nrf2 유도제와 억제제 모두 항암 정책으로 가치가 있을 수 있음은 분명합니다.
그럼에도 불구하고 Nrf2의 조절 효과로 인해 항암제의 해독 과정에 활성이며 암세포에서 활성화되면 화학 내성이 생길 수 있습니다.
암세포에서 Nrf2의 유익하거나 불리한 과정은 기본적으로 그 작용, 종양 주변 및 세포 유형의 긴밀한 제어에 달려 있습니다[ 117 ].
지난 10년 동안 Nrf2는 암 예후 및 치료에서 중요한 바이오마커로 알려져 왔습니다[ 118 ].
암 환자에서 Nrf2의 높은 발현은 항암제와 방사선 요법에서 가장 높은 이점을 얻지 못했습니다 [ 119].
Nrf2 매개 유전자 발현에 대해 확립된 위험 점수 시스템은 암 환자의 무재발 생존 및 전체 생존에 대한 평가를 제공하기 위해 확립되었습니다.
Nrf2는 OS에 대한 방어를 제공하고 종양 촉진 및 진행을 예방하는 데 중요합니다[ 125 , 126 ].
연구에 따르면 Nrf2가 녹아웃된 유기체는 독성 물질에 노출된 후 중요한 장기에 더 큰 손상을 입힙니다.
Nrf2는 ARE를 통한 전사 활성화를 통해 산화 조직 손상 및 염증을 안정화합니다.
폐기종 발병에서 Nrf2의 보호 활성은 담배 연기로 인한 Nrf2 녹아웃 마우스를 테스트하여 관찰되었습니다[ 128 ]. 폐기종은 담배 연기에 노출된 지 8주에 처음 발견되었고 16주 후에 악화되었지만 대조군에서는 병리학적 기형이 발견되지 않았습니다. 결과는 Nrf2가 산화제/항산화제 균형을 조정하여 폐기종의 발병을 방어할 수 있음을 보여줍니다.
ROS와 RNS는 만성 염증이 암 유발 변화에 기여하는 주요 원인으로 여겨집니다[ 130 ].
Nrf2는 치료 저항성, 개선된 항산화 능력 및 공격적인 종양 형성 능력을 포함하여 암세포에 무한한 이점을 보여주기 때문에 Nrf2가 활성화된 암세포는 종종 "Nrf2 중독"을 발전시킵니다.
Nrf2의 지속적인 자극은 암세포의 성장과 생존에 도움이 되지만, 정상 세포에서 Nrf2의 높은 자극은 매우 유독합니다.
이러한 발견은 명확한 요구 사항이 Nrf2 중독 암의 형성을 허용한다는 것을 시사합니다[ 137 ].
Nrf2 유도제를 사용한 암 치료는 암세포에서 Nrf2 자극의 잠재적인 악성 발달 결과를 유발할 수 있습니다.
고맙게도 Nrf2에 중독된 암세포에 대한 Nrf2 유도제의 효과는 미미한 것으로 추정됩니다.
Nrf2의 억제는 Nrf2 중독 암 치료를 위한 고무적인 접근 방식입니다.
그럼에도 불구하고, 전신 Nrf2 억제제를 사용하는 것은 세포 보호에서 Nrf2의 필수적인 역할을 보고 암 보유 숙주에 원치 않는 영향을 미칠 수 있습니다.
'전사인자' 카테고리의 다른 글
| NRF2 신호 전달 경로의 치료 표적화 (0) | 2021.10.20 |
|---|---|
| NRF2 억제제의 잠재적 응용 (0) | 2021.10.20 |
| Nrf2: 양날의 검 (0) | 2021.10.20 |
| HIF-1a를 표적으로 하는 최근 약제 -2012년 (0) | 2021.10.20 |
| HIF-1 표적 (0) | 2021.10.20 |