2019
Understanding the relevance of herb–drug interaction studies with special focus on interplays: a prerequisite for integrative medicine
(상호 작용에 특별한 초점을 맞춘 허브-약물 상호 작용 연구의 관련성 이해: 통합 의학의 전제 조건)
https://europepmc.org/article/pmc/pmc6726296
Understanding the relevance of herb-drug interaction studies with special focus on interplays: a prerequisite for integrative me
Abstract Integrative medicine refers to the blending of conventional and evidence-based complementary medicines and therapies with the aim of using the most appropriate of either or both modalities for ultimate patient benefits. One of the major hurdles fo
europepmc.org
HDI의 메커니즘
HDI는 약력학 및/또는 약동학 메커니즘에 의해 매개됩니다.
약동학적 상호작용은 약력학적 상호작용보다 예측하기가 훨씬 더 어렵습니다.
가장 일반적으로 보고되는 HDI는 약동학적 상호작용, 특히 주로 사이토크롬(CYP); P-gp와 같은 약물 수송체; 및 단백질 결합의 drug-metabolizing enzyme(DME)의 기능적 조절로 인해 발생하는 상호작용입니다.
. 반면, 약력학적 상호작용에는 길항작용, 추가/합산, 상승작용 및 때로는 약물 표적의 조절이 포함됩니다.
그러나 다른 유형의 상호 작용, 즉 약동학 및 약력학 상호 작용을 유발할 수 있는 다중/복합 HDI가 있을 수 있으며 cytokines–hormones–neurotransmitter–enzymes–transporter (CHNET) 변경과 관련된 상호 작용을 통해 매개될 수도 있고 아닐 수도 있습니다.
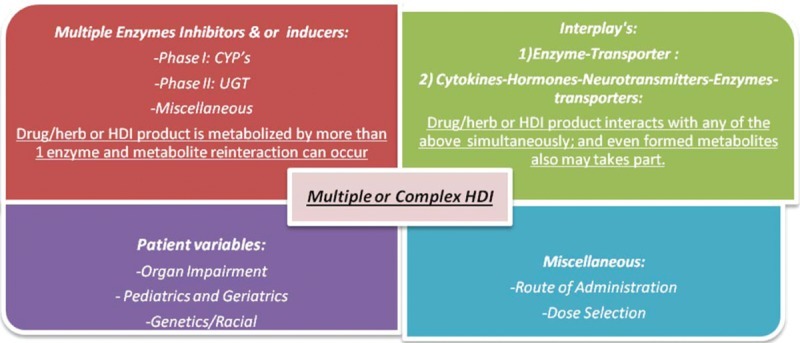
그림그림1은 HDI의 개요를 제공하고 그림그림2 는 HDI의 메커니즘을 설명합니다.

허브-약물 상호작용 개요:
허브-약물 상호작용(HDI)은 복합 HDI(CHDI)를 유발할 수 있는 약물 및/또는 허브의 약동학(PK)-약력학(PD)에 직간접적인 영향을 미칩니다.
HDI의 유형과 강도는 PRF:SADI(Patient-related factors: sex, age, disease/disorder, and individualization)의 간접적인 역할과 함께 고려 중인 약초 및 약물의 특성에 따라 다릅니다(환자 관련 요인: 성별, 연령, 질병/장애 및 개별화).
참고: 직선은 주요 유형 및/또는 주요 효과를 나타내는 반면 점선은 배경 상호 작용/효과를 나타냅니다.
GIT =위장관, NTW=좁은 치료 창.
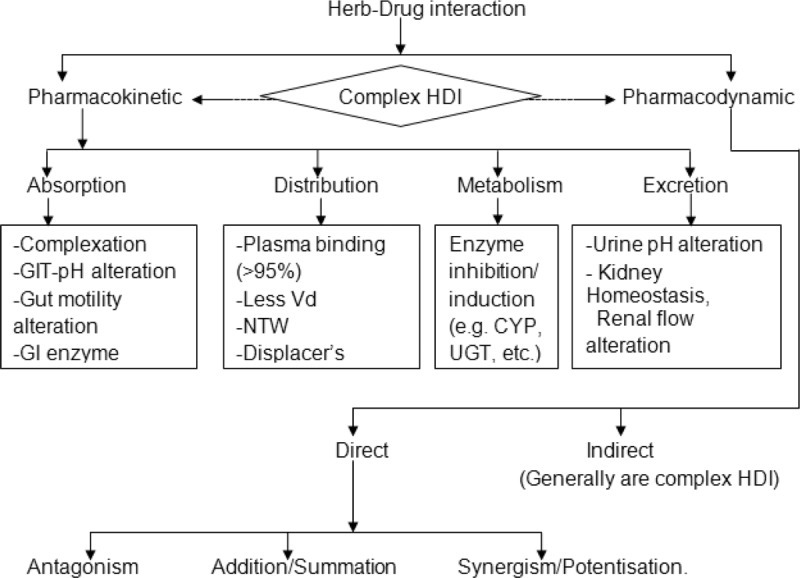
허브 약물 상호 작용의 메커니즘.
CYP=cytochrome, GIT=gastrointestinal tract, Vd=volume of distribution, UGT=UDP-glucuronosyltransferase.
약동학적 HDI
약동학적 HDI는 섹션별로 설명된 흡수, 분포, 대사 및 배설(ADME)의 모든 단계에서 발생할 수 있습니다. 테이블1 번 테이블1몇 가지 대표적인 예를 다룹니다.
Table 1
Pharmacokinetic–pharmacodynamic HDIs

정상적인 위장관 환경에 영향을 미치는 모든 허브는 약물의 예상되는 흡수 패턴의 변화에 결정적 요인며 HDI를 유발할 것입니다(그림 1 참조).그림 1흡수 상자).
예를 들어, 허브 완하제 또는 벌크 형성제는 장의 통과를 가속화하여 장의 흡수를 방해할 수 있습니다.
가장 인기 있는 완하제 허브는 센나( Cassia senna 및 C angustifolia ) 및 cascara sagrada( Rhamnus purshiana )와 같은 안트라노이드 함유 허브입니다.
또한, 위의 pH를 증가시키는 제산제, 전신 항궤양제 부류에 속하는 약물의 존재하에 약산성 한약 추출물/제제의 흡수가 영향을 받을 수 있으며 그 반대의 경우도 마찬가지입니다.
이러한 상호작용은 혈장 단백질 결합 특성이 더 높고(>95%), Vd(volume of distribution=분포 부피)가 적으며, 치료 범위=narrow therapeutic window(NTW)가 좁은 약물에서 발생할 수 있습니다.
예를 들어 잘 알려진 와파린은 98% 혈장 단백질에 결합되어 0.11~0.18 L/kg의 Vd와 1~2의 NTW로 유지되며 이는 시토크롬 P450(CYP450) 효소의 다형성=polymorphism에 따라 다릅니다.
와파린과 상호작용하는 약제의 알려진 예로는 비타민 K, 일부 유형의 차 및 녹색 잎 채소가 있습니다.
Agrimonia eupatoria 는 항응고제의 효능을 방해하는 것으로 보고되었습니다.
이러한 약제는 와파린의 효과를 증가 또는 감소시켜 각각 출혈을 연장하거나 혈액 응고의 위험을 증가시켜 와파린과 상호 작용합니다.
따라서 HDI는 치명적일 수 있는 엄청난 위험을 내포하므로 와파린을 복용하는 환자는 허브를 동시에 복용하는 동안 극도로 주의해야 합니다.
예를 들어, 건강한 피험자에서 와파린의 PK-PD는 은행나무와 생강의 권장 복용량에서 미미한 영향을 받았습니다.
Echinacea는 S-warfarin의 혈장 농도를 상당히 감소시킵니다.
St John's wort는 warfarin의 항응고 효과를 감소시키는 반면, Allium sativum 은 출혈 위험을 증가시킵니다.
신진 대사는 일반적으로 동일한 것을 제거하기 위해 특수 효소 시스템을 통해 살아있는 유기체에 의한 xenobiotics의 생화학적 변형입니다.
대사율은 약물의 약리작용의 지속시간과 강도를 결정합니다.
전신 순환에 접근할 수 있는 많은 수의 식물화학물질은 친유성 경향이 있어 결과적으로 배설하기 어렵습니다.
따라서 신체는 배설을 촉진하기 위해 신진 대사를 통해 친수성을 만듭니다.
이것은 2단계로 이루어지며, 1상은 약물/생체생물체를 산화, 환원 또는 가수분해하는 CYP450 동종효소 시스템을 포함하는 반면, 2상은 각각 극성 부분인 글루쿠로네이트, 아세테이트 및 설페이트와 약물의 수용해도를 증가시키는 글루쿠론화, 아세틸화 및 황산화 반응과 같은 접합 반응을 포함합니다.
테이블표2 ㄴㅡㄴ기능적 역할과 함께 중요한 대사 효소를 다룹니다.
많은 DME는 성별, 연령, 질병/장애 및 개별화와 같은 환자 관련 요인과 관련하여 다형성 특성 및 강도가 다양함을 보여줍니다(PRF:SADI).
Phytochemicals/xenobiotics는 DME의 간 및 간외 발현을 조절하여 HDI를 유발하는 약물의 대사에 현저한 변화를 일으킬 수 있습니다.
이러한 사실을 고려하여 FDA(Food and Drug Administration)에서는 약물 상호작용 데이터를 요구합니다.
인간 약물 대사에서 개별 CYP 효소의 중요성은 다양하며, CYP3A, CYP2D 및 CYP2C가 대부분의 의약품/이물질의 대사를 각각 50%, 25% 및 20% 담당합니다. 허브 성분은 유도 및/또는 억제를 통해 대사 효소를 변경할 수 있습니다.
허브 제품에 의한 CYP 유도에는 일반적으로 며칠이 소요됩니다.
그러나 효소의 유도는 약물 혈장 수준을 감소시키고(약물 대사 증가를 통해) 결과적으로 약물 효과를 감소시킬 수 있습니다.
반대로, CYPs의 억제는 종종 즉각적이며 약물 혈장 수준을 증가시킬 수 있으며(약물 대사 감소를 통해) 약물 효과를 강화하여 심각한 부작용이나 독성을 초래할 수 있습니다.
전구약물의 경우 유도와 억제 모두 반대 현상이 발생할 수 있습니다.
많은 임상 부작용이 CYP 매개 HDI와 관련이 있는 것으로 보고되었습니다.
대사성 약동학적 HDI는 다양한 메커니즘에 의해 발생합니다.(그림 3).

대사 약동학 허브 약물 상호 작용.
Vmax=maximum reaction velocity in enzyme kinetics,
효소 역학에서 최대 반응 속도
Km=the substrate concentration required to produce half Vmax in enzyme kinetics.
효소 역학에서 Vmax의 절반을 생성하는 데 필요한 기질 농도.
동일한 CYP isoform에 의해 종종 대사되기 때문에 허브 성분과 약물 간에 상호 경쟁 억제가 발생할 수 있습니다.
예를 들어, 마늘의 디알릴 설파이드는 CYP2E1의 경쟁적 억제제입니다.
비경쟁적 억제는 친전자성 그룹(예: 이미다졸 또는 히드라진 그룹)을 포함하는 허브 성분이 CYP의 헴 부분에 결합함으로써 발생합니다.
예를 들어, 피페린은 비경쟁 메커니즘에 의해 CYP1A 및 CYP2A를 억제합니다.
St John's wort에 존재하는 Hyperforin은 CYP2D6의 강력한 비경쟁적 억제제이기도 합니다.
CYP의 메커니즘 기반 억제는 고려 중인 CYP와 허브 대사 산물 사이의 복합체 형성으로 인한 것입니다.
예를 들어, 디알릴 설파이드에서 파생된 디알릴 설폰은 CYP2E1의 자가 촉매적 파괴를 유도하는 에폭사이드 대사 산물을 통해 복합체를 형성함으로써 CYP2E1의 자살 억제제 입니다 .
따라서 CYP2E1에 의해 대사되는 약물은 마늘과의 병용 투여 시 주의해서 복용/모니터링할 필요가 있습니다.
약물/제노바이오틱의 반응성 대사산물의 형성은 독성과 관련이 있음이 분명합니다.
생약 대사체에 의해 매개되는 독성은 대부분 세포독성, 종양유전자 활성화, 과민반응과 같은 여러 경로 를 통해 발생합니다.
예를 들어, 예를 들어, Aristolochia spp.에 존재하는 Aristolochic acid는 CYP1A1/2 매개 생물 활성화를 일으키고, 이는 H-ras 종양유전자를 활성화시키고 결국 발암을 일으키는 니트레늄 이온을 생성합니다.
유사하게 민간요법인 Germander( Teucrium chamaedrys )는 방부제 및 날씬한 다이어트 보조제로 사용되었습니다.
1991년에 저먼더는 간독성과 치명적인 것으로 밝혀졌습니다.
Germander에 존재하는 디테르페노이드의 푸란 고리는 CYP3A4에 의해 대사되어 반응성 에폭사이드 라디칼을 형성합니다. 이러한 에폭사이드 라디칼은 CYP3A 및 에폭사이드 수산화효소와 반응하여 미토콘드리아 투과성 전이, 카스파제 활성화 및 간세포의 세포자멸사를 추가로 유발합니다.
제거 상호 작용
신체에서 약물이 제거되는 소스는 소변, 대변, 땀, 눈물, 정액, 월경 분비물 등입니다. 약물 또는 생체이물 제거의 주요 주체는 P-gp, 유기 음이온 수송 폴리펩타이드(OATP)와 같은 세포 수송 단백질/효소입니다. ), 유기 음이온 수송체, OCTP, 유방암 저항성 단백질 등이 이 과정에 있습니다. 그러나 이들은 약초와 약물의 병용 투여에 의해 영향을 받아 HDI를 유발할 수 있습니다. 43 또한, 일부 허브는 이뇨제로 알려져 있어 약의 배설에 영향을 줄 수 있습니다. 116신독성 약물은 신장 손상을 유발하여 제거 속도가 느려 체내에 허브와 약물이 축적됩니다. 신장을 손상시키는 약물의 중요한 예로는 겐타마이신, 암포테리신 B, 메토트렉세이트 및 토브라마이신이 있습니다. 따라서 원치 않는 HDI를 방지하기 위해 면밀한 모니터링이 필요합니다. 더욱이, 제거 상호작용의 경우 수송자가 세포 안팎으로 생체이물의 수송을 지배하므로 수송자의 역할에 초점을 맞출 필요가 있습니다.
DME보다 덜 알려져 있지만, 막 수송체는 약물/약초의 PK-PD에 중요한 영향을 미칠 수 있습니다. 그러나 간과 장에 주로 집중되어 있는 DME와 달리 수송체는 신체의 모든 조직에 다양하게 존재하며 약물의 흡수, 분포, 조직 특이적 약물 표적화 및 제거에 중요한 역할을 합니다(그림 2a). .(그림 44).10,101,117

약물의 흡수, 분포, 대사 및 배설에 관여할 수 있는 장벽(A), 간(B) 및 신장(C)의 유출 및 흡수 수송체의 예.
BCRP = 유방암 저항성 단백질, MATE = 다제 및 독성 화합물 압출 단백질, MDR1 = 다제내성 1(P-당단백질(P-gp)),
MRP = 다제내성 관련 단백질, OAT = 유기 음이온 수송체, OATP= 유기 음이온 수송 폴리펩타이드,
OCT = 유기 양이온 수송체, PEPT1 = 펩타이드 수송체 1.
현재까지 확인된 대부분의 수송체는 ATP 결합 카세트, 즉 P-gp 및 용질 운반체의 2가지 수퍼 패밀리 중 하나에 속합니다.
운반체와 DME는 기질 특이적 상호작용(due to substrate overlapping=기질 겹침으로 인해)을 나타내며 서로의 기능적 효능에 영향을 미칠 수 있습니다.
P-gp는 주로 약물 제거 기관에서 발견되는 원형질막 결합 약물 유출 단백질이며 아마도 P-gp가 신체에서 생체이물을 적극적으로 배출 하기 때문에 해독 수송체로 기능할 것입니다.
소장에서 P-gp는 장 상피 세포의 정점 막에 국한되어 화합물을 장 내강으로 다시 유출시키는 역할을 합니다.
mdr1a 녹아웃 마우스에서 paclitaxel 및 digoxin의 약동학 연구는 이러한 약물의 경구 생체이용률을 제한하는 데 장내 P-gp의 중요성을 보여주었습니다.
파이토케미컬은 또한 장내 P-gp 및 약물의 유출을 촉진하는 기타 다제내성 단백질과 같은 ATP 의존성 수송체 단백질과 상호작용하는 것으로 알려져 있습니다.
다양한 약물(예: 퀴니딘, 베라파밀 및 이트라코나졸)이 장 수준에서 유출 수송체 P-gp를 억제함으로써 디곡신의 혈장 수준을 증가시키는 것으로 나타났습니다.
rosuvastatin, pravastatin 및 pitavastatin을 포함한 많은 β-Hydroxy β-methylglutaryl-CoA 환원효소 억제제의 혈장 농도는 cyclosporine, rifampin 및 flavonoid와 같은 간 흡수 수송체 억제제(예: OATP1B1)의 병용 투여에 의해 증가합니다.
케르세틴, 커큐민 등과 같은 일반적으로 발견되는 허브 성분은 OATP1B1/1B3의 경쟁적 억제제입니다.
이 범위에서 Tucker 등은 전송자 수준에서 HDI를 예측하는 능력을 향상시키기 위한 다양한 핵심 사항을 논의했습니다.
다중/복합 HDI: HDI 맥락에서 상호작용의 중요성
ADME 및 수송체와 관련된 HDI는 별도로 논의되었지만 그러나 어떤 경우에는 다중/복합 HDI라고 하는 이러한 메커니즘의 조합에 의해 약물 상호 작용이 발생할 수 있으며 이러한 시나리오에는 다음이 포함되지만 이에 국한되지는 않습니다.
-
(1)1개의 효소의 동시 억제 및 유도 또는 약물 및/또는 허브에 의한 효소 및 수송체의 동시 억제
-
(2)약물 및/또는 허브를 대사하는 동일한 효소의 1개 이상의 억제제를 사용하여 약물 제거 억제 증가
-
(3)약물 및/또는 허브를 대사하는 하나 이상의 효소 억제제를 사용하여 약물 제거 억제 증가
-
(4)기질 약물 및/또는 허브를 대사하는 효소를 억제하는 약물 및 그 대사산물에 의한 억제
-
(5)두 효소에 의해 대사되는 기질을 취하는 대사 불량자에서 유전적 다형성 효소 이외의 효소 억제
-
(6)생체이물을 제거하는 장기(예: 간 또는 신장) 손상 정도가 다양한 대상에서 효소/수송체 억제제 사용.
그러나 HDI에 여러 메커니즘이 관련된 경우 상호 작용이 발생할 수 있습니다.
일반적으로 인터플레이가 증가함에 따라 HDI의 복잡성도 증가합니다.
그림5-다중/복합 HDI의 다양한 방법을 설명합니다.
사분면의 크기는 해당 사분면의 예상 기여도를 반영합니다.
상호작용은 2개 이상의 사물이 서로 영향을 미칠 때 발생한다고 합니다. 위에서 논의한 바와 같이 HDI에 기여하는 약물의 ADME에 영향을 미치는 많은 요인이 있습니다. 이러한 교란 요소 및/또는 ADME 플레이어가 서로 영향을 미치거나 기질이 겹치면 상호 작용이 발생합니다. 가장 많이 연구되고 일반적인 상호작용은 효소-수송체 상호작용입니다.
DMEs-transporter interplays=DME-수송체 상호작용
한약은 종종 경구 투여되며 장내강(대부분의 경구 투여 약물의 주요 흡수 부위) 및 간에서 중등도 내지 고농도에 도달할 수 있으며 장세포 및 간세포에 상당한 영향을 미칠 수 있습니다.
P-gp와 CYP3A4는 모두 장세포와 간세포의 융모 끝에서 풍부하게 발현됩니다.
장내 P-gp와 CYP3A4의 상호작용은 사이클로스포린, 미다졸람, 탈리놀롤, 스타틴, HIV 프로테아제 억제제 및 베라파밀을 포함한 대부분의 경구 투여 약물의 생체이용률에 강력한 영향을 미칩니다.
많은 연구에 따르면 CYP3A4와 P-gp는 모두 보조 기질을 가지고 있으며 정점 유출 펌프 P-gp와 상호 작용하는 약물은 장 분비 해독 동안 기질의 CYP3A4 매개 소실을 향상시킬 수 있습니다.
P-gp 뿐만 아니라 협력 방식으로 첫 번째 통과 대사에 영향을 미칠 수 있습니다.
따라서, 한약에 의한 장 및 간 P-gp 및 CYP3A4의 조절은 병용 약물의 생체 이용률이 조절될 수 있는 잠재적으로 중요한 기전을 나타냅니다.
시간 의존적 HDI는 주로 형성된 1차 대사산물에 의존하며, 이는 일반적으로 동일한 모 대사 효소와 상호작용하고 시간 의존적 및/또는 농도 의존적이며 궁극적으로 복합 HDI를 담당하는 억제 또는 유도를 유도합니다(그림 . 4)
반대로, CYP3A4와 P-gp 사이의 상호작용을 지지하는 증거는 주로 제한된 시험관 내 및 전임상 연구에서 비롯되며 일반적으로 인간에 대해 외삽됩니다.
이러한 PK 상호작용은 약력학적 반응을 변경할 수 있습니다.
또한 사이토카인, 호르몬, 신경 전달 물질, 효소 및 수송체가 모두 상호 작용하여 복잡한 상호 작용을 일으켜 잠재적인 HDI를 유발할 수 있는 경우가 있을 수 있습니다.
사이토카인-호르몬-신경전달물질-효소-수송체 상호작용
사이토카인, 호르몬, 신경 전달 물질, 효소 등과 같은 내인성 분자 간의 상호 작용은 피드백 루프와 건강한 상태를 통해 정상적인 항상성을 유지하는 데 중요합니다.
이 상호작용은 DME와 전송기의 기능적 능력에도 간접적으로 영향을 미칩니다.
질병에 걸린 상태에서 이 상호작용이 변경되고 이러한 결함으로 인해 전체 CHNET 상호작용이 변경되고 때로는 투여된 약물의 PK-PD에 영향을 미칩니다. (그림 6그리고7).
CHNET 상호작용은 단순히 DME-수송자 상호작용과 비교하여 연구하고 사용하기가 매우 어렵습니다(그림.(그림 6그리고7).
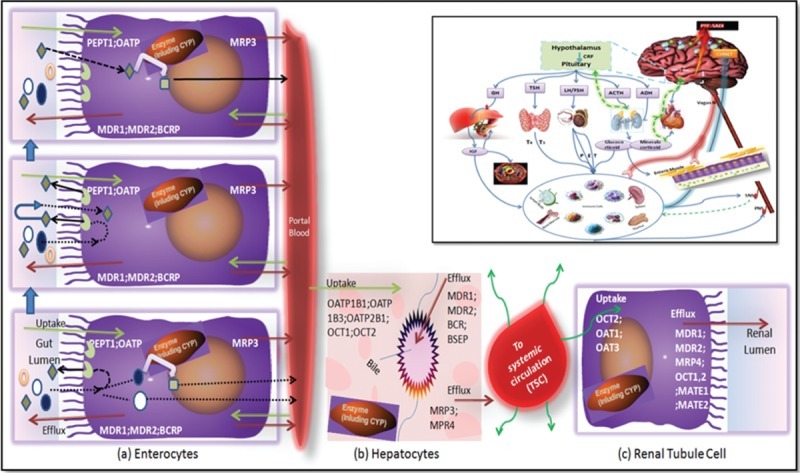
상호작용:
(A) 장세포에서 CYP3A4와 P-당단백질 상호작용,
(B) 간세포,
(C) 신세뇨관 세포 및 포함된 작은 사각형에는 PRF: SADI가 포함됩니다(환자 관련 요인: 성별, 연령, 질병/장애, 개별화) 이는 CHNET의 불균형 수준의 결과로 정상적인 생리적 균형의 변화를 담당합니다.
이는 최종적으로 약물 상호 작용(HDI)에 의해 단일 약물의 변경된 약동학(PK)-약력학(PD) 및 심지어 DI/허브에 기인한 약물 이상 반응/약물 이상 반응(ADE/ADR) 및/또는 의심되지 않는 심각한 이상 반응(SUSAR)의 발생에 대한 책임이 있습니다.
예를 들어 당뇨병에서는 CYP2C11의 발현이 감소하고, 및 CYP2E1 증가는 인슐린 및 기타 호르몬의 변화된 수준 뿐만 아니라 정상적인 신체 생리학의 변화에 의해 유발되거나 수행되었을 수 있으며 이로 인해 유익/유해/심지어 치명적일 수 있는 모든 HDI 또는 DI가 발생합니다.
그림 A는 장에서 CYP3A와 P-당단백질 사이의 상호작용에 대한 개념을 설명합니다.
세 가지 약물 분자가 표시됩니다(

). 그들은 모두 동일한 약물이며 결과에 따라 다릅니다.
약물은 효소에 의해 대사될 수 있는 장세포로 수동적 과정에 의해 흡수됩니다.
그러나, 약물은 또한 장으로 다시 능동 유출될 수 있으므로 후속 수동 흡수 시 효소에 추가로 접근할 수 있습니다.
비어있는 원(

) 분자는 장세포로 들어가고 CYP3A에 의해 대사되지 않거나 P-당단백질에 의해 내강으로 다시 유출됩니다. 그런 다음 간문맥에서 간으로 진행됩니다.
고체 원(

) 분자는 장세포로 흡수되고 효소와 처음 만날 때 열린 사각형 생성물로 대사됩니다.
열린 사각(

) 대사 산물은 간문맥혈이나 장내강으로 되돌아갑니다.
그러나 음영 처리된 다이아몬드 분자는 흡수됩니다(

). 이들은 효소에 의해 대사되지 않습니다. 이것은 P-당단백질(

)에 의해 장내강으로 다시 유출 되고 이 순환은 장세포로 네 번째 진입할 때 음영 처리된 다이아몬드 분자가 대사되는 곳에서 다시 한 번 발생합니다.
유입 수송체는 운반체 매개 및/또는 활성 수송체, 심지어 Hsp(

)와 같은 다른 물질에 의한 약물 분자의 흡수를 돕습니다. Hsp는 수용체에 약물/리간드를 부착하는 동안 도움이 됩니다.
예를 들어 Hsp는 방향족 탄화수소 수용체에 결합하는 동안 도움이 되며 특히 스트레스 동안 단백질의 합성, 수송 및 접힘=folding에 주요 역할을 합니다.
이 그림은 전달자가 효소에 대한 약물의 접근을 제어하여 효소에 온전한 생체이물이 혈류로 들어가는 것을 방지할 수 있는 여러 기회를 제공한다고 설명합니다.
따라서 효소, 수송체 및 기타 단백질 및 비단백질 분자는 외부 물질을 몸 밖으로 내보내는 보호 과정으로 coordinated=상호조정된 방식으로 작동합니다.

약동학에 대한 사이토카인-호르몬-신경전달물질-효소-수송체(CHNET) 상호작용의 효과:
질병 및/또는 질병 동안 CHNET의 균형 잡힌 네트워크가 변경되고 투여된 약물의 전체 약동학(PK)-약력학(PD)에 영향을 미칩니다.
실선은 상응하는 대응물에 대한 기능적 발현/능력에 대한 직접적인 영향을 나타내고 점선은 ROS, NF-kB, gp-130 등과 같은 다른 요인의 관여를 통한 간접적인 영향을 보여줍니다.
CAR = 구성 안드로스탄 수용체, NF-kB = 핵 인자 -kappaB,
NRs = 다음과 같은 기타 핵 수용체:FXR, NR1H4,
PRF: SADI = 환자 관련 요인: 성별, 연령, 질병 및 개별화, PXR = 임신 X 수용체, ROS =활성산소종.
Shapiro LE와 Shear NH는 약리학적 요인, 다약제, 장기 기능 장애 외에도 약리학적 위험 요인 및/또는 개별화가 HDI에 영향을 미친다는 점을 검토했습니다.
정상적인 신체 생리학적 상태를 유지하는 데 CHNET이 중심적인 역할을 하며 질병/건강하지 않은 상태의 환자에서 이것이 변경되어 정신 생리학적 사회적 행동뿐만 아니라 수용체 약리학을 변화시키고 새로운 수용체 표적을 유도할 수 있습니다 .
따라서 많은 리뷰어와 연구자들이 수행한 연구에서 환자의 정상적인 정신생리학적 상태를 변화시키는 외부 요인과 함께 숙주-미생물군-바이로바이오타 간의 항상성과 상호작용 사이에 강한 관계가 있을 수 있다는 결론을 내릴 수 있습니다.
마지막으로, 이 모든 것 때문에 CHNET의 수준과 강도가 변경되어 궁극적으로 DI/HDI와 함께 약물의 정상적인 PK-PD에 영향을 미치는 개별화된 CHNET 캐스케이드를 생성합니다.
이러한 관찰은 약물-질병-약물/약초 상호작용에 초점을 맞춘 주제에 대한 새로운 시각을 요구합니다.
약력학적 HDI
약력학적 상호작용은 주로 수용체 수준에서 발생하며 직접 및 간접 HDI로 분류됩니다(그림 1b).(그림 2).
직접 HDI는 간접 HDI보다 이해하기 쉽고 예측하기도 쉽습니다.
약물은 이러한 약리학적 활성을 공유하는 식이 보조제/한약재와 함께 사용할 때 더 위험할 수 있습니다.
직접적인 상호작용의 몇 가지 예가 표에 언급되어 있습니다.1 번 테이블.
간접 약력학적 HDI의 좋은 예 중 하나는 와파린의 항응고 활성을 강화하는 크랜베리입니다.
혈장 약물 농도가 두 배로 증가하면 치료 및 안전 범위에 따라 약물 효과 및/또는 부작용이 강화될 수 있습니다.
그러나 급격한 농도-반응 관계 또는 좁은 치료 지수를 가진 약물의 경우 덜 현저한 변화가 여전히 임상적으로 중요할 수 있습니다.
HDI의 임상적 중요성은 병용 약물/약초(용량, 투여 요법, 투여 경로, 약동학 및 치료 범위) 및 PRF:SADI와 관련된 요인에 따라 다릅니다.
즉, 약초와 약물 상호작용의 정도는 약물 대사 및 수송체의 개별화, 다른 약물과의 복약, 연령 및 기타 많은 요인에 따라 개인마다 크게 다릅니다.
--------------------------------------------------------
HDI 예측은 DDI 예측보다 더 어려운 것으로 보입니다.
그러나 다음 기준이 충족될 때 시험관 내 대사 억제 데이터에서 식물 성분-약물 상호 작용 및/또는 DDI 예측에 약간의 성공이 있었습니다
-
(1)약물 제거는 주로 대사에 의해 이루어져야 합니다.
-
(2)약물은 실질적인 접합 또는 기타 비-CYP 대사의 대상이 아닙니다.
-
(3)간은 대사 제거의 주요 기관입니다.
-
(4)이 화합물은 흡수 문제(즉, 제한된 용해도, 낮은 위장 투과성)와 관련된 물리화학적 특성을 가지고 있지 않습니다.
그러나 HDI의 예측은 다음 요인에 의해 장애가 될 수 있습니다.
(1) 한약은 종종 전체 제형으로서 DME, 수송체 및 수용체에 대한 억제 및/또는 유도 효능과 함께 활성 성분의 상이한 양적 존재를 갖는 수백 가지 성분을 포함합니다.
(2) CHNET의 하나 이상의 구성 요소 간의 상호 작용으로 인해 간접 HDI가 관련된 일부 경우;
(3) 약초에 의한 CYP 및 P-gp의 억제 및/또는 유도(관련 교란 요인에 따라 달라질 수 있음);
(4) 많은 약초가 만성적으로 사용됩니다.
(5) 품질 관리 문제로 인해 허브 성분의 활성 함량에 상당한 변동성;
(6) 간외 대사의 존재; 및 간에서의 능동 수송;
(7) PRF:SADI.
이러한 모든 요소는 HDI의 최종 결과에 기여할 것입니다.
IM 개발, HDI 검사 및 예측에 직간접적으로 도움이 될 수 있는 중국 전통 의학 시스템과 Ayurveda를 기반으로 하는 여러 소프트웨어와 웹 사이트가 있습니다(표(표3).
표 3
허브-약물 상호작용 연구에 유용한 데이터베이스 100

Good Practice in Traditional Chinese Medicine (GP-TCM)
- Phytochemical Databases of Chinese Herbal Constituents & Bioactive Plant Compounds with Known Target Specificities
TCM Database paper - research from King's College London - Phytochemical Informatics of Traditional Chinese Medicine & Therapeutic Relevance
Chemiformatics paper - research from King's College London - TCM-ID Database (Singapore)
TCM-ID Database (Singapore) - TCMGeneDIT Database (Taiwan)
TCMGeneDIT Database (Taiwan) - Virtual Screening of Chinese Herbs with Random Forest
Chemiformatics paper - research from King's College London - Web-based TCM Information database
Traditional Chinese Medicine Information Database
- CIMR: Core Information for Metabolomics Reporting
including a list of publications on technical details of metabolomics and chemical analysis - European Charter for Researchers
- GP-TCM Checklist for Consistent and Acceptable Quality of Herbal Research Materials
- GP-TCM Definition to Good Practice in TCM Research
- GP-TCM Good Practice Guidelines on Reviewing and Publishing Studies on Herbal Medicine, with Special Emphasis on Traditional Chinese Medicine and Chinese Materia Medica
- GP-TCM Guidelines for Randomized Controlled Trials Investigating Chinese Herbal Medicine (CHM) - Summary
- GP-TCM Guidelines for Randomized Controlled Trials Investigating Chinese Herbal Medicine (CHM) and a Summary to This Guideline
- GP-TCM Position on Good Practice in TCM Research
- MIAME: Minimum Information About a Microarray Experiment
- MIAPapAE: Minimum Information About a Peptide Array Experiment
Please also visit: http://journal.embnet.org/index.php/embnetjournal/article/view/250/715 - MIAPE: Minimum Information About a Proteomics Experiment
including a 'parent' document laying out principles and a number of 'modules' (MS, MSI & GE, etc) each of which applies to a particular technology - MIARE: Minimum Information About a RNAi Experiment
- MIBBI Bioscience Reporting Guidelines and Tools
Some MIBBI guidelines of particular interest (MIQE, CIMR, MIAME, MIAPE, MIAPapAE and MIARE) are listed independently below. For a full range of MIBBI guidelines and tools, please visit - MIQE: Minimum Information for Publication of Quantitative Real-Time PCR Experiments
- The European Agency for Safety and Health at Work Guidelines
- The Quest for Modernisation of TCM
- Wellcome Trust Guidelines on Good Research Practice
- British Pharmacological Society
- CAMbrella consortium
EC - FP7 funded Coordination Action Project for complementary and alternative medicine - Consortium for Globalisation of Chinese Medicine (CGCM)
- European Medicines Agency (EMA)
- International Society of Chinese Medicine
- International Society of Ethnopharmacology
- Medicines and Healthcare products Regulatory Agency (MHRA)
- Society for Medicinal Plant and Natural Product Research
- State Food and Drug Administration, P. R. China (SFDA)
- The International Society of Regulatory Toxicology & Pharmacology
- U.S. Food and Drug Administration (FDA)
미래 전망
약물-질병-약초 상호작용
몇 가지 중요한 DME 및 수송체의 발현과 활동은 소아, 노인, 임신, 신부전 및 간부전과 같은 특수 인구 및/또는 조건에서 변경됩니다.
이제 PK-PD의 변화는 다양한 병태생리학적 조건에서도 발생할 수 있다는 것이 잘 받아들여졌습니다.
약물-질병-약초 상호작용을 이해하려면 질병 관점에서 약물유전학적-약물 상호작용 데이터에 초점을 맞출 수 있는 도구/기술이 필요합니다 .
토론 및 결론
가장 널리 사용되는 Ayurvedic rasayana 식물 중 하나인 T cordifolia 와 cyclophosphamide의 수성 줄기 추출물을 동시에 투여하면 cyclophosphamide의 약동학에 영향을 미치지 않으면서 골수 억제를 크게 역전시킬 수 있음을 보여주었습니다.
그들은 그러한 연구가 암 등과 같은 만성 질환에 대한 보조 치료를 설계하는 데 매우 도움이 될 수 있다고 덧붙였습니다.
Hudson et al 212MSKE와 레스베라트롤이 전립선암 세포 성장 억제에 대해 별도로 연구되었을 때 MSKE와 레스베라트롤은 전립선암 세포 성장을 억제하는 별개의 경로를 표적으로 삼았음에도 불구하고 무스카딘 포도 껍질 추출물(MSKE)이 레스베라트롤을 함유하고 있음을 보여주었습니다.
따라서 주요 식물 성분만으로는 전체 추출물의 효과 또는 약리학적 반응을 확실히 예측할 수 없습니다.
********************************************************************************
2012
https://www.frontiersin.org/articles/10.3389/fphar.2012.00069/full
An overview of the evidence and mechanisms of herb–drug interactions
허브-약물 상호작용의 증거 및 메커니즘 개요
An Overview of the Evidence and Mechanisms of Herb–Drug Interactions
Despite the lack of sufficient information on the safety of herbal products, their use as alternative and/or complementary medicine is globally popular. There is also an increasing interest in medicinal herbs as precursor for pharmacological actives. Of se
www.frontiersin.org
약초 제품은 약리학적으로 활성인 식물화학물질의 복잡한 혼합물로 만들어지며, 대부분은 시키메이트, 아세테이트-말로네이트 및 아세테이트-메발로네이트 =shikimate, acetate–malonate, and acetate–mevalonate 경로를 통해 생성된 2차 대사산물입니다.
이러한 구성성분에는
phenolics (such as tannins, lignins, quinolones, and salicylates), p
henolic glycosides (such as flavonoids, cyanogens, and glucosinolates),
terpenoids (such as sesquiterpenes, steroids, carotenoids, saponins, and iridoids),
alkaloids,
peptides,
polysaccharides (such as gums and mucilages), r
esins, and essential oils 등이 있습니다.
이러한 복잡성은 임상 약물 상호 작용의 위험을 증가시킵니다.
허브-약물 상호작용의 메커니즘
생리학적 시스템의 생체 변형 경로에서 기질 특이성이 겹치는 것은 약물-약물, 식품-약물 및 HDI의 주요 원인으로 간주됩니다.
수용체 부위와 상호작용하고 생리학적 환경을 변경하는 다양한 화학적 모이어티의 능력은 약력학적 약물 상호작용을 설명할 수 있는 반면, 약동학적 상호작용은 변경된 흡수, 분포 패턴의 간섭, 대사 및 배설 경로의 변화 및 경쟁에서 발생합니다.
약물-약물 상호작용과 같은 약동학적 HDI의 주요 기본 메커니즘은 장 및 간 대사 효소, 특히 CYP 효소 계열의 유도 또는 억제입니다.
또한, 약물 수송체 및 유출 단백질, 특히 장의 p-당단백질에 대한 유사한 효과가 대부분의 다른 경우에 원인이 됩니다(.
CYP 및 유출 단백질의 전신 활성은 종종 경구 생체이용률에 영향을 미치므로 함께 투여되는 허브 제품의 조절 활성은 영향을 받는 약물의 혈중 농도를 현저하게 감소 또는 증가시키는 것으로 나타났습니다.
생체 내 약물 상호 작용의 가능성은 간 효소 에 대한 시험관 내 연구 에서 종종 추론됩니다 . 시험관 내 결과와 생체 내 행동 의 상관 관계는 임상적으로 유의미한 정도가 거의 추론할 수 없지만 생체 내 예측 가능성 측면에서 특정 사례에서 신뢰할 수 있는 결과를 산출했습니다 .
따라서 후속 섹션에서 볼 수 있듯이 잘 확립된 HDI의 대부분은 초기 에 시험관 내 연구를 통해 입증되었습니다.
허브 제품과 간 효소의 상호 작용은 약력학적 효과를 유발할 수도 있습니다.
식물 화학 물질에 의해 유발될 수 있는 특정 간 손상에는 아미노전이효소의 증가, 급성 및 만성 간염이 포함됩니다,간부전, 정맥 폐쇄 장애, 간경변, 섬유증, 담즙정체, 구역 또는 미만성 간 괴사 , 지방증이 포함됩니다.
간 손상의 메커니즘에는 CYP의 생물학적 활성화, 산화 스트레스, 미토콘드리아 손상 및 세포자멸사가 포함될 수 있습니다.
대사효소 유도 및 억제
CYP 슈퍼패밀리는 일반적으로 생체이물과 내인성 화합물의 산화, 과산화 및 환원적 생체 변형에 관여합니다.일반적으로 염기서열 상동성을 기반으로 패밀리와 서브패밀리로 나뉜다.
다양한 패밀리들 사이에 기질 특이성이 높습니다.
패밀리 1, 2 및 3에 속하는 CYP는 주로 생체이물 대사에 관여하는 반면 다른 것들은 호르몬, 담즙산 및 지방산과 같은 내인성 화합물의 형성 및 제거에 중요한 역할을 합니다.
인간에서 약물 대사를 담당하는 가장 중요한 CYP 서브패밀리는 1A2, 2A6, 2C9, 2C19, 2D6, 2E1, 3A4 및 3A5입니다.
CYP1A1 및 1A2는 인간 CYP1A 서브패밀리의 두 가지 주요 구성원입니다.
CYP 1A1은 주로 신장, 장, 폐와 같은 간외 조직에서 발현되는 반면 CYP1A2는 전체 간 CYP의 약 15%를 구성합니다.
CYP2B6은 약물 대사에 관여하는 반면 CYP2B 서브패밀리의 대부분의 다른 구성원은 덜 중요한 대사 역할을 합니다.
서브패밀리 2C는 인간 간에 존재하는 총 CYP의 20% 이상을 나타내는 3A 다음으로 두 번째로 풍부한 CYP입니다.
2C8, 2C9 및 2C19의 세 가지 활성 구성원으로 구성되며 모두 레티놀과 레티노산을 포함한 일부 내인성 화합물의 대사에도 관여합니다.
파라세타몰, 클로르족사존 및 엔플루란을 포함하여 임상적으로 관련된 약물은 2E 서브패밀리 중 가장 활성인 CYP2E1에 의해 대사됩니다(.
CYP3A 서브패밀리는 인체의 총 CYP의 40% 이상을 구성하며(수준은 개인마다 40배 다를 수 있음) CYP3A4는 간과 장에서 고도로 발현되는 모든 동형 중 가장 풍부하며 오늘날 사용되는 약물의 절반의 대사에 참여합니다.
이들 효소에 대한 기질 및 억제제의 특이성 및 선택성은 약동학 및 독성학 연구에서 특히 유용합니다.
유도는 증가된 mRNA 전사의 결과로 장 및 간 효소 활성이 증가하여 정상적인 생리학적 값보다 높은 단백질 수준을 초래합니다.
이런 일이 발생하면, 경구 생체이용률과 전신적 소인 모두에 영향을 미치는 약물 대사 속도의 상응하는 증가가 있습니다.
특정 허브 제품은 CYP를 유도할 수 있는 것으로 나타났습니다.
효소 유도 외에도 허브 제품은 효소 활성을 억제할 수도 있습니다.
CYP 및 기타 대사 효소의 억제는 일반적으로 즉각적 및 억제제 농도 의존적 효과와 경쟁적입니다.
대부분의 억제제는 CYP의 기질이기도 합니다.
예상되는 전신성 장 및 간 대사의 억제 결과, 비정상적으로 높은 혈장 수준의 생체 이물이 관찰됩니다.
독성 발현은 이 관찰의 궁극적인 효과일 수 있습니다.
효소 억제의 동등하게 임상적으로 중요한 결과는 억제된 간 청소율로 인한 약물 축적입니다.
이러한 효과는 치료 범위가 좁거나 용량-반응 프로파일이 가파른 약물에서 특히 문제가 될 것입니다.
St John's wort는 가장 널리 사용되는 허브 항우울제 중 하나입니다.
이는 CYP3A4의 강력한 유도제이며 투여량, 기간 및 투여 경로에 따라 다른 CYP 동종효소 및 P-gp를 유도하거나 억제할 수 있습니다.
사례 보고서의 연구에 따르면 CYP3A4에 대한 유도 효과로 인해 사이클로스포린, 심바스타틴, 인디나비르, 와파린, 아미트립틸린, 타크롤리무스, 옥시코돈 및 네비라핀을 포함한 CYP3A4 기질의 혈장 수준을 상당히 감소시키는 것으로 나타났습니다.
또한 SJW로 인한 사이클로스포린의 혈청 농도 변화로 인해 환자의 장기 거부 반응이 발생한 것으로 보고되었습니다.
SJW와 경구 피임약 간의 상호 작용으로 인한 돌발성 출혈 및 계획되지 않은 임신에 대한 보고도 문서화되었습니다.
세르트랄린 및 파록세틴과 같은 SSRI와 함께 사용하면 중추 세로토닌성 증후군의 증상이 나타나는 것으로 보고되었습니다.
또한 톨부타미드의 약동학적 프로파일에 명백한 변화 없이 톨부타미드를 복용하는 환자의 저혈당 발생률을 증가시키는 것으로 알려져 있습니다.
또한 암 환자에서 이리노테칸의 활성 대사산물인 SN-38의 생성을 억제합니다.
Amitriptyline은 CYP3A4와 장내 P-gp의 기질입니다.
따라서 CYP3A4 의존성 대사 활성의 유도로 인해 치료 실패의 위험이 높아서 경구 생체이용률이 낮습니다.
2주 동안 SJW 추출물과 아미트립틸린을 병용 투여한 12명의 우울증 환자에서 아미트립틸린의 혈장 농도-시간 곡선 아래 면적의 21% 감소가 관찰되었습니다.
SJW에 의해 약동학적 프로파일이 변경된 것으로 보고된 다른 CYP 및 P-gp 기질에는 펜프로쿠몬 및 와파린과 같은 항응고제; 펙소페나딘과 같은 항히스타민제; 프로테아제 억제제 및 역전사효소 억제제를 포함하는 항레트로바이러스 약물; 톨부타미드와 같은 혈당강하제; 사이클로스포린, 타크로리무스 및 미코페놀산과 같은 면역억제제; 카르바마제핀과 같은 항경련제; 이리노테칸과 같은 항암제; 테오필린과 같은 기관지 확장제; 덱스트로메토르판과 같은 진해제; 스타틴, 디곡신 및 디히드로피리딘 칼슘 채널 차단제와 같은 심혈관 약물; 경구 피임약; 메타돈 및 로페라미드와 같은 아편제; 및 알프라졸람 및 미다졸람을 포함한 벤조디아제핀.
인간에서 5% 하이퍼포린을 함유한 SJW의 표준화된 추출물 300mg을 단일 용량 투여한 후, [ I ]/ K i > 0.22 를 산출하는 0.17-0.5μM 하이퍼포린의 최대 혈장 농도 에서 생체 내 외삽법이 생체 내에서 발생할 가능성이 높음을 시사합니다.
약동학적 약물 상호작용에서 SJW가 다양한 CYP 효소를 조절한다는 것을 동물 연구를 통해 확인했습니다.
SJW가 미다졸람의 증가된 요 청소율 관찰을 통해 건강한 대상에서 CYP3A4를 유도할 수 있음을 입증했습니다.
따라서 동물 및 인간 연구는 SJW가 다양한 CYP 동종효소에 대한 억제 및 유도 성분을 모두 함유하고 있음을 추가로 확인합니다.
이러한 효과는 투여량과 투여 기간에 따라 달라질 수 있으며 종 및 조직에 따라 다를 수도 있습니다.
SJW의 개별 식물화학적 성분은 CYP 동종효소의 대사 활성에 다양한 효과를 나타내지만, 전체 추출물 및 주요 구성 성분, 특히 하이퍼포린은 시험관 내 연구 및 생체 내 연구를 통해 CYP1A2, 2C9, 2C19, 2D6 및 3A4의 대사 활성을 억제하는 것으로 보고되었습니다.
은행나무 는 건강한 인간 대상에서 CYP 2C19 의존성 오메프라졸 대사를 유도하는 것으로 보고되었습니다.
마늘-사퀴나비르 상호작용 연구에서 마늘의 존재로 인한 사퀴나비르 경구 생체이용률의 51% 감소와 마늘 유도 CYP3A4 유도에 기인한다고 보고했습니다.
와파린 약동학에 미치는 영향은 동물 모델에서도 보고되었습니다.
자몽 주스가 의약 목적으로 소비되지는 않지만, CYP에 대한 플라보노이드 함량의 억제 활성이 발견되면서 플라보노이드를 함유한 약초 요법에서 HDI 가능성이 밝혀진 약초에 대한 추가 연구가 이어졌습니다
관련된 CYP 억제제는 로테논입니다. 헴철(heme iron)의 전자 전달을 방해함으로써 jicama 덩굴 식물과 같은 여러 식물에서 발견되는 자연 발생 식물화학물질인 rotenone은 CYP 활성을 억제하는 것으로 알려져 있습니다.
천연 고분자인 레스베라트롤과 아미노산인 트립토판은 강력한 CYP 억제제로 보고되었습니다
CYP와 상호 작용할 수 있는 일부 약초 및 식물 화학 성분이 표 3 에 나와 있습니다.
HDI에서 CYP의 보다 자세한 관련은 최근에 발표된 일부 리뷰에 자세히 설명되어 있습니다
( Delgoda and Westlake, 2004 ; Pal and Mitra, 2006 ; Cordia and Steenkamp, 2011 ; Liu et al., 2011 ).
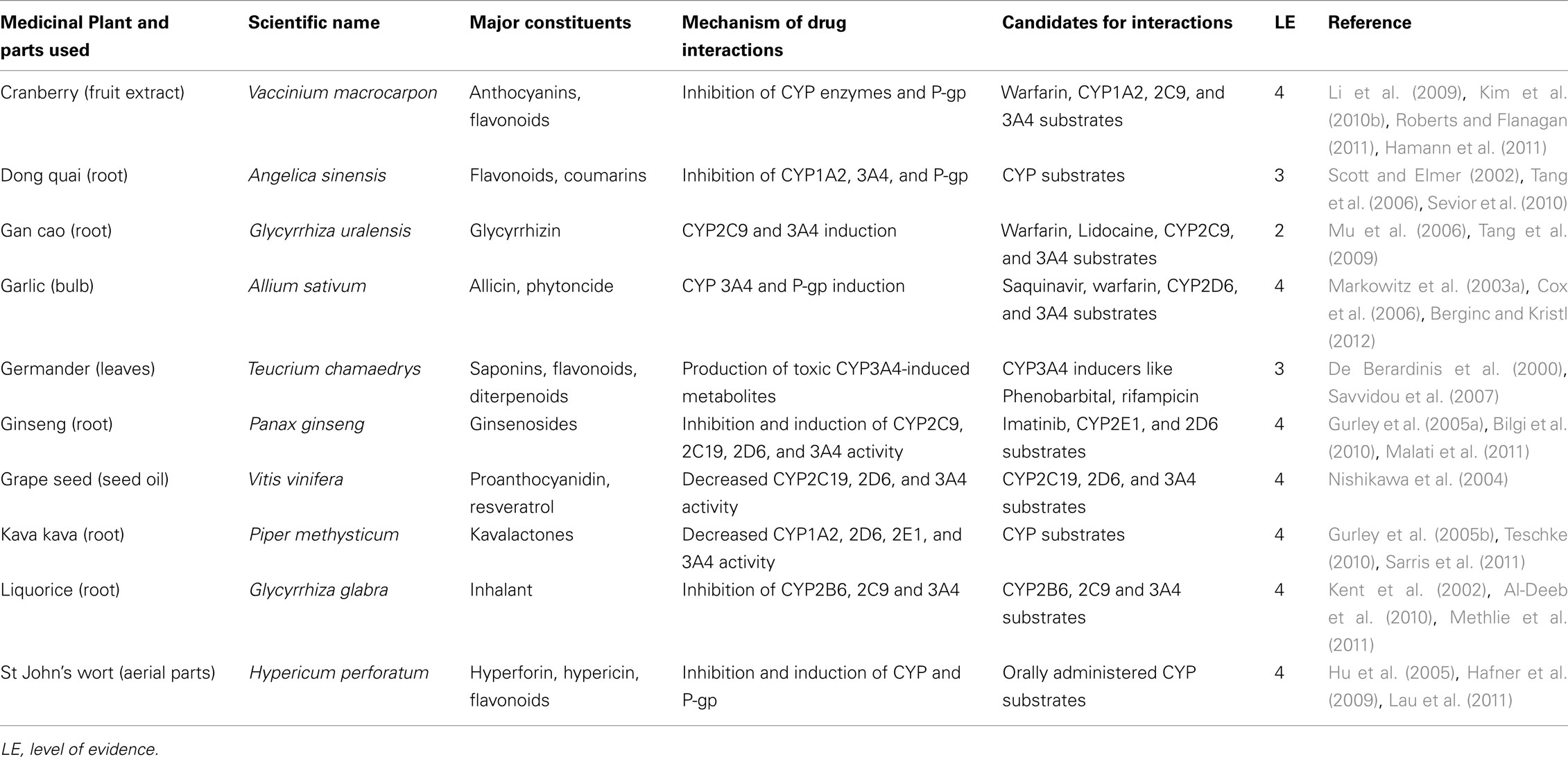
표 3 . CYP 및 유출 단백질과 상호 작용하는 것으로 알려진 일부 허브 제품 .
우리딘 디포스포글루쿠로노실 트랜스퍼라제(UGT), N- 아세틸 트랜스퍼라제(NAT), 글루타티온 S- 트랜스퍼라제(GST) 및 설포트랜스퍼라제(ST)를 포함한 2상 대사 효소는 제거를 돕는 1상 대사산물에 극성 및 이온화 가능한 그룹의 부착을 촉매합니다.
사이토크롬 P450 매개 HDI가 다양한 연구에서 광범위하게 조사되었지만, 제2상 효소에 대한 허브 추출물의 효과는 적절하게 연구되지 않았습니다.
그러나 임상적으로 유의한 HDI를 유도하는 II상 효소의 가능성을 시사하는 충분한 증거가 문헌에 있습니다.
저혈당 허브인 , Cymbopogon proximus, Zygophyllum coccineum 및 Lupinus albus 의 추출물 은 GST와 GSH의 활성을 감소시켰습니다.
항염증 및 항종양 특성을 지닌 허브 항산화제인 Curcuma longa 의 Curcumin 은 ddY 생쥐 간에서 GST와 퀴논 환원효소의 활성을 증가시켰습니다.
허브 수면 보조제인 발레리안(Valerian)도 UGT의 억제를 통해 HDI를 유도할 수 있는 가능성을 보여주었습니다.
쥐오줌풀 추출물에 의한 UGT 활성 억제의 최대 87%가 에스트라디올과 모르핀을 프로브 기질로 사용한 시험관 내 연구에서 보고되었습니다(.
앞서 설명한 바와 같이 은행나무 가 CYP 효소에 미치는 잘 알려진 효과 외에도 , 그 추출물은 인간의 간과 장내 마이크로솜에서 조사된 마이코페놀산 글루쿠론산화의 강력한 억제를 입증했습니다.
Mohamed and Frye(2011b) 는 녹차 유래 에피갈로카테킨 갈레이트에 의한 UGT1A4 억제를 보고했습니다.
밀크씨슬에 의한 UGT 1A6 및 UGT1A9; 쏘팔메토의 UGT 1A6; 및 크랜베리의 UGT 1A9. 최근 간행물은 UGT에 의해 매개되는 잠재적인 HDI의 증거를 제시합니다.
쿠마린, 리메틴, 아우랍텐, 안젤리신, 베르가모틴, 임페라토린 및 이소핌피넬린을 포함한 특정 식물화학물질도 간 GST 활성을 유도할 수 있는 것으로 보고되었습니다.
이러한 발견의 임상적 중요성은 아직 결정되지 않았지만 2상 대사 효소가 HDI에서 중요한 역할을 할 수 있다는 점은 주목할 만합니다.
수송 및 유출 단백질의 억제 및 유도
ATP 결합 카세트(ABC) 약물 수송체 계열은 약물의 흡수, 분포 및 제거에 중요한 역할을 합니다.
이 패밀리에서 가장 많이 연구된 구성원인 P-gp는 인간 MDRI 유전자에 의해 암호화된 170kDa 혈장 당단백질입니다.
그것은 많은 신체 조직에서 구성적으로 발현되며 간의 담즙 소관의 정점 상피 표면, 신장의 근위 세뇨관, 췌관 세포, 소장의 원주 점막 세포, 결장 및 결장 및 부신. 그것은 장, 신장, 뇌에서 약물의 흡수와 제거에 적극적으로 관여합니다.
특히 이러한 단백질은 약물과 그 대사물의 간담도, 직접 장 및 소변 배설 과정에 관여합니다.
따라서, P-gp의 조절, 또는 동시 투여된 허브에 의한 결합 부위에 대한 기질로서의 경쟁적 친화도는 약물의 약동학적 프로파일의 변경 가능성을 제시합니다.
약동학적 상호작용은 한약이 경쟁적 또는 비경쟁적 메커니즘을 통해 약물 수송체의 정상적인 활성 수준을 억제하거나 감소시킬 때 발생합니다.
상호작용은 또한 관련 단백질의 mRNA의 증가를 통한 수송 단백질의 유도를 통해 발생할 수 있다.
연구에서 플라보노이드, 퓨라노쿠마린, 레세르핀, 퀴니딘, 요힘빈, 빈크리스틴, 빈블라스틴 등의 식물화학물질을 포함한 임상적으로 중요한 P-gp 억제제가 다수 확인되었습니다
valinomycin, nonactin, nigericin, monensin, calcimycin 및 lasalocid와 같은 이동성 이온 전달 물질은 P-gp에 의한 안트라사이클린의 유출을 억제하는 반면 gramicidin과 같은 채널 형성 이온 전달 물질은 그렇지 않다고 보고했습니다.
CYP와 상호작용하는 여러 허브 제품도 수송 단백질에 유사한 영향을 미칩니다(표 3 ).
수송 단백질은 항암제의 약동학에 적극적으로 관여하며, 화학요법제에 대한 암세포의 다중 내성의 잘 알려진 메커니즘 중 하나를 설명합니다.
일부 허브가 수송 단백질에 미치는 영향은 표 4 에 나와 있습니다..
약초와 화학요법제 간의 임상적으로 관련된 상호 작용은 Yap et al.의 최근 리뷰에 자세히 설명되어 있습니다. (2010) .

표 4 . 수송 단백질에 대한 허브 제품의 영향 .
위장 기능의 변화
장내 대사 효소와 유출 단백질에 미치는 영향 외에도, 한약은 여러 메커니즘을 통해 동시에 투여되는 약물의 흡수를 변경할 수 있습니다.
위장 pH 및 기타 생화학적 요인의 변화는 케토코나졸 및 이트라코나졸과 같은 pH 의존성 약물의 용해 특성 및 흡수를 변경할 수 있습니다.
복합화 및 킬레이트화, 불용성 복합체 형성 및 흡수 부위에서의 경쟁, 특히 부위 특이적 제형과의 경쟁은 약물의 흡수에 큰 영향을 미칠 수 있습니다.
Anthranoid-containing plants - 계수나무 ( 계수나무 senna ), 계수나무 ( Rhamnus purshiana ), 대황 ( Rheum officinale), 구아검과 차전자피를 포함한 가용성 섬유는 GI 통과 시간을 줄여 약물 흡수를 감소시킬 수 있습니다.
그들은 GIT 운동성을 증가시키는 것으로 알려져 있습니다.
처방된 약물과 함께 사용하는 경우 위장관 통과 시간 감소로 인해 약물의 흡수에 상당한 변화가 있는 것으로 보고되었습니다
안트라노이드가 Na + /K + ATPase를 억제하고 산화질소 합성효소의 활성을 증가시켜 장 상피에 해로울 수 있음을 입증했습니다 .
이것은 장내 수분과 염분 흡수의 변화와 그에 따른 체액 축적으로 인해 장 통과를 상당히 증가시켰습니다.
마늘 유래 화합물은 쥐의 위장관에서 quinone reductase와 glutathione transferase의 조직 활성을 증가시키는 것으로 나타났습니다.
신진대사에서의 역할을 고려할 때 두 효소는 특히 화학 발암 물질로부터 화학 보호 작용을 하는 것으로 간주됩니다.
CYP 및 P-gp 매개 메커니즘 외에도 잘 알려진 인삼 유도 약동학 HDI는 위장 효과, 특히 위 분비 억제 효과 때문일 수 있습니다.
난용성 약물인 furosemide의 흡수를 증가시키는 rhein과 danthron의 잠재력은 시험관 내 연구를 통해 입증되었습니다.
한약재인 쥐를 대상으로 한 연구에서,Polygonum paleaceum 은 위장관의 운동성을 억제하고 배변 반사를 억제하며 위 배출을 지연시키는 잠재력을 보여주었습니다.
유사한 연구 에서 위장 운동에 대한 두 가지 중국 전통 약초 처방인 Fructus aurantii immaturus 와 Radix paeoniae alba 의 억제 효과가 입증되었습니다.
페녹시메틸페니실린, 메트포르민, 글리벤클라미드 및 로바스타틴과 같은 약물의 흡수는 담즙산의 격리를 통해 고섬유질 허브 제품에 의해 감소될 수 있습니다
신장 제거의 변화
여기에는 신장 기능과 상호 작용할 수 있는 허브 제품이 포함되어 약물의 신장 제거가 변경됩니다.
이러한 상호작용은 세뇨관 분비 억제, 세뇨관 재흡수 또는 사구체 여과 방해로 인해 발생할 수 있습니다허브 이뇨의 메커니즘은 복잡하고 균일하지 않습니다. 특정 허브는 사구체 여과율을 증가시키지만 전해질 분비를 자극하지 않는 반면 일부 허브는 직접적인 세뇨관 자극제로 작용합니다.
신장 기능 및 약물 제거와 상호 작용할 수 있는 일부 허브는 표 5 에 나와 있습니다.
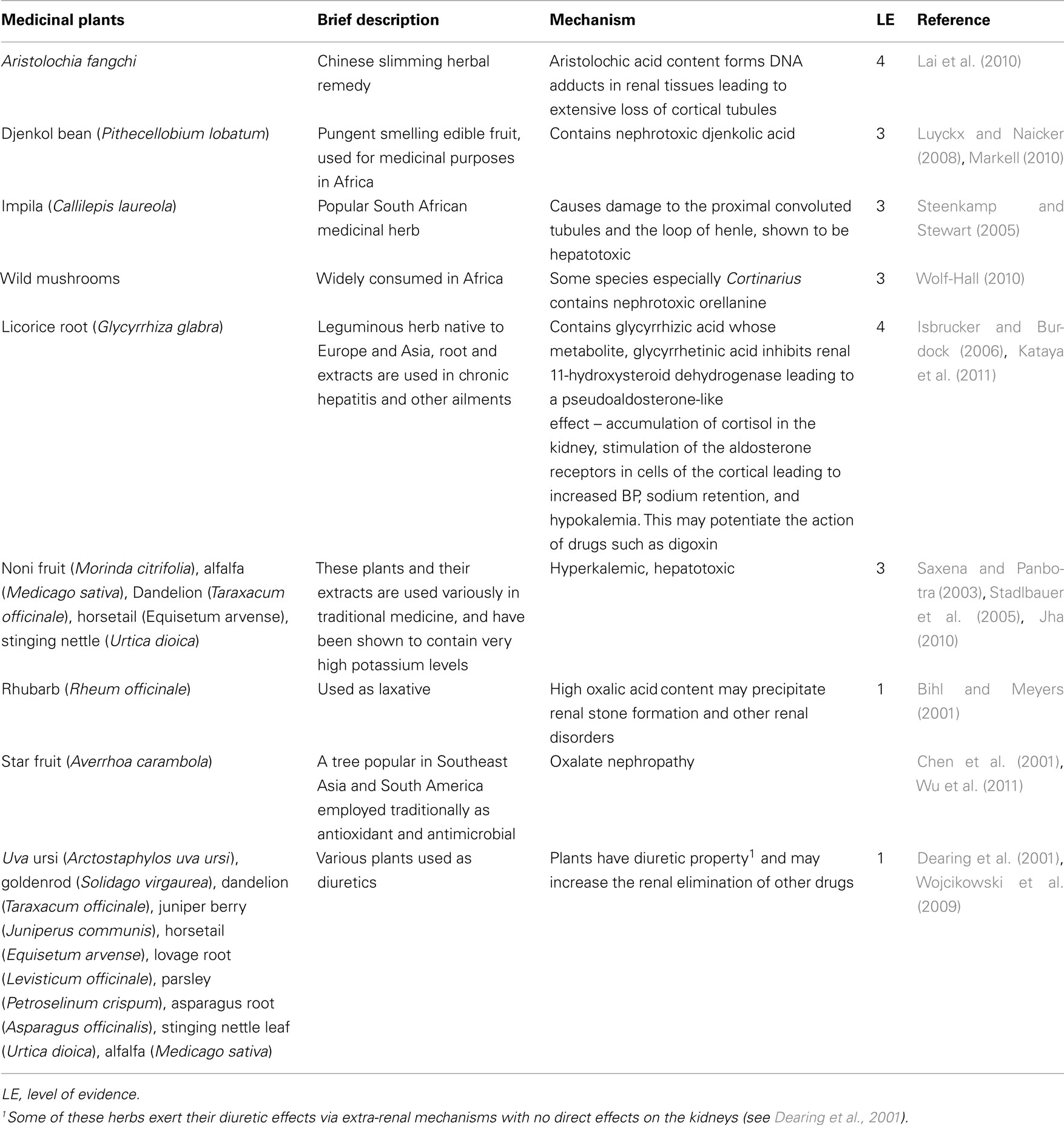
표 5 . 신장 기능의 변경을 통해 다른 약물과 상호 작용할 수 있는 일부 약초 요법 .
약력학적 시너지, 첨가, 길항작용
약초-약물 상호 작용은 공통 수용체 부위에 대한 친화성의 결과로 약초 제품과 기존 약물의 상승 작용 또는 부가 작용을 통해 발생할 수 있습니다.
이는 약력학적 독성 또는 길항 효과를 유발할 수 있습니다(표 6 ).
대부분의 다른 허브와 마찬가지로 SJW에는 phenylpropanes, naphthodanthrones, acylphloroglucinols, flavonoids, flavanol glycosides, and biflavones=페닐프로판, 나프토단트론, 아실플로로글루시놀, 플라보노이드, 플라바놀 배당체 및 비플라본을 포함한 식물 화학 물질의 복잡한 혼합물이 포함되어 있습니다.
하이퍼포린은 신경전달물질(도파민, 세로토닌, 노르아드레날린)의 재흡수를 억제하는 것으로 알려져 있으며 SJW의 항우울 활성을 담당하는 생리활성 물질로 여겨집니다.
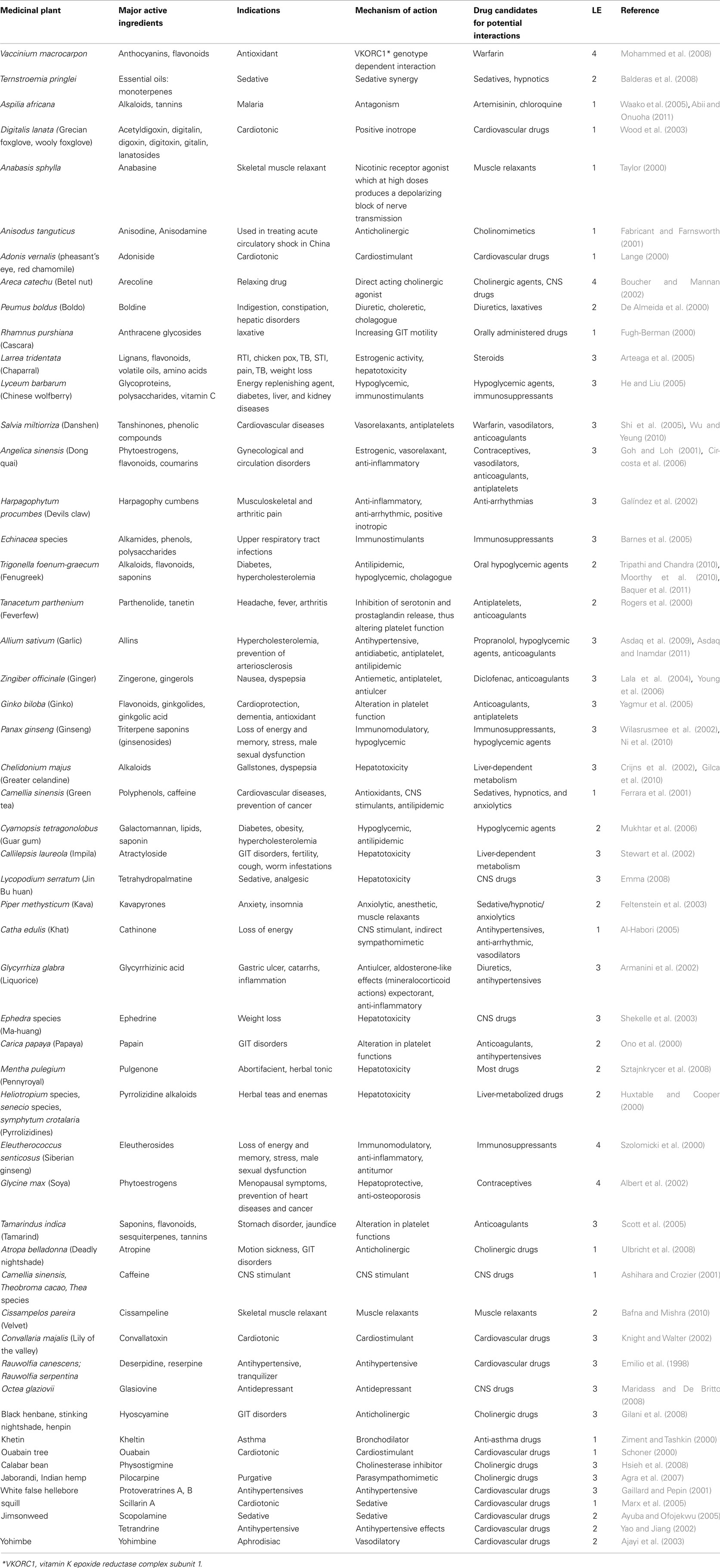
표 6 . 허브 제품과 기존 약물 간의 약력학적 상호 작용의 몇 가지 예 .
******************************************************************************************
'약물' 카테고리의 다른 글
| 임상 증상을 기반으로 한 허브 및 기존 약물 상호 작용의 현재 관점 (0) | 2022.09.14 |
|---|---|
| 허브-약물 상호 작용: 메커니즘 및 임상 측면의 개요 (0) | 2022.09.14 |
| 약물대사(약동학, 약력학)-국외 (0) | 2022.09.10 |
| 약물대사(약동학, 약력학)-국내 (0) | 2022.09.09 |
| 허브-약물 상호작용 및 독성 (0) | 2022.09.08 |