2021
Multifaceted Factors Causing Conflicting Outcomes in Herb-Drug Interactions
https://www.mdpi.com/1999-4923/13/1/43/htm
Multifaceted Factors Causing Conflicting Outcomes in Herb-Drug Interactions
Metabolic enzyme and/or transporter-mediated pharmacokinetic (PK) changes in a drug caused by concomitant herbal products have been a primary issue of herb and drug interactions (HDIs), because PK changes of a drug may result in the alternation of efficacy
www.mdpi.com
허브-약물 상호작용에서 상충되는 결과를 야기하는 다면적 요인
한약재(HD)의 조합은 한약재와 약물 간의 약리학적 효과의 간섭으로 인해 예상치 못한 효과(예: 약효 손실 또는 독성 증가)를 초래할 수 있으며, 이를 한약재 상호작용(HDI)으로 정의합니다.
약초 제품에 의한 약물(예: 와파린, 인슐린, 아스피린, 디곡신 또는 사이클로스포린)의 약동학 변화는 주로 대사 효소 및/또는 수송체의 억제 또는 유도에 의해 매개되며, 이는 결과적으로 약리 작용의 변화를 유발할 수도 있습니다.
약초 제품이 약물의 PK에 영향을 미치는 대사 효소 및/또는 수송체를 조절하면 약물의 혈장 및/또는 조직 농도가 변경되어 약리학적 또는 독성학적 효과에 예기치 않은 변화가 발생합니다[.
2. HDI를 유발하는 주요 경로: 대사 효소 및 운반체 매개 HDI
허브 제품은 체내 흡수, 분포, 대사 및/또는 배설(ADME) 과정에서 약물과 동일한 대사 경로 및 수송 시스템을 활용합니다( 그림 1 ).
Tsai et al. HDI 사례의 약 43%가 PK 기반 상호 작용과 관련이 있으며 HD 조합으로 인한 금기 사례가 발생했다고 보고했습니다.
약동학 기반 약물-약물 상호작용(DDI)의 평가에서 관심 약물은 대사 효소 및/또는 수송체의 기질(희생 약물) 또는 억제제 또는 유도제(가해자 약물) 역할을 했습니다[
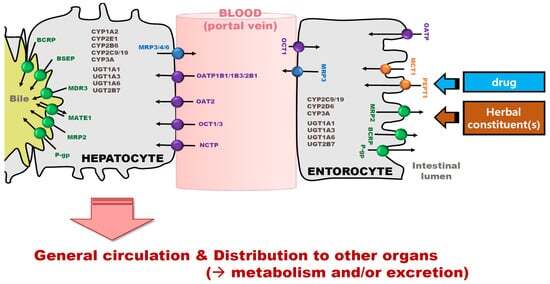
그림 1. 약물 및 생약 제품의 수송체 및 대사 효소 매개 성향 패턴.
막을 가로질러 조직으로 들어가는 약초 제품의 약물 또는 화학물질(예: 장세포의 apical membrane, 간세포의 sinusoidal membrane 또는 신장 근위 상피 세포의 basolateral membrane)은 수동 확산 및/또는 수송체에 의해 조절됩니다.
그런 다음 허브 제품의 약물 및 화학 물질은 I 및 II 단계 대사 효소 및/또는 운반체 매개 배설(예: 신장 또는 담즙 배설)을 통한 대사에 의해 제거됩니다.
특히, 중요한 PK 매개변수인 생체이용률은 장 흡수 및 유출 수송체, 장 대사 효소 및 간 흡수로부터의 대사를 포함하는 초회 통과 효과의 결과로 가변적입니다.
이에 비해 분포, 대사 및 배설의 변화는 주로 각 조직에서 흡수 및 유출 수송체의 조절 및/또는 대사 효소의 억제/유도를 통해 발생합니다.
PK 기반 HDI를 유발하는 기본 메커니즘으로 , 먼저 허브 제품은 각각 수송체 또는 대사 효소에 영향을 미칩니다.
장세포의 apical membrane에서 약초 제품에 의한 수송체의 억제는 약물의 수송체 매개 유출을 감소시키고 결과적으로 약물(예: 은행나무 및 밀크씨슬)의 흡수를 증가시킵니다.
밀크씨슬은 간과 신장에서 P-gp 억제제(P-gp)로 작용하는 허브 제품으로, 약물의 담즙 배설과 신장 배설을 변경할 수 있습니다.
결과적으로 혈장 농도를 증가시켜 약물에 대한 전신 노출을 증가시킵니다.
또한, 한방 제품은 전신 노출 변화와 함께 병용 약물의 제거에 영향을 미치는 대사 효소를 억제하거나 유도합니다.
특정 수송체 또는 대사 효소에 대한 생약 제품의 논란의 여지가 있는 효과(즉, 억제 및 유도 효과)가 보고되었습니다.
St. John's Wort 추출물의 만성 동시 투여는 St. John's Wort에 의한 CYP 3A의 유도를 통해 midazolam의 혈장 농도를 감소시켰지만 St. John's Wort 추출물의 단일 투여는 CYP 3A4를 억제했습니다.
둘째로, 허브 제품은 수송체와 대사 효소에 동시에 영향을 미칩니다.
허브 제품에 의해 변형된 수송체와 대사 효소는 때때로 시너지 가능성을 보여줍니다.
일부 허브 제품(예: 마늘, 은행, 인삼 및 포도 주스)은 P-gp 억제제와 CYP3A 억제제 모두의 기능을 합니다.
장세포에서 한약재에 의한 P-gp 및 CYP3A 억제는 경구 투여된 약물에 대한 전신 노출을 증가시키는 것으로 보고되었습니다 .
밀크씨슬은 장에서 경구 투여된 사이클로스포린 A의 P-gp 매개 유출 및 CYP3A 매개 대사를 억제하여 사이클로스포린 A의 경구 생체이용률을 증가시킵니다.
또 다른 예로서, 허브는 간에서 P-gp를 억제하고 간에서 담즙으로의 약물 유출을 감소시키는 반면, CYP3A 억제제로서 약물의 CYP3A 매개 대사를 감소시켜 간과 혈장에서 약물 농도를 증가시킬 수 있습니다.
피페린이나 캡사이신과 같은 파이토케미컬과 독소루비신의 병용투여는 독소루비신의 담즙 배설 및 간 대사를 억제하여 결과적으로 간 및 혈장 내 독소루비신 농도를 증가시켰다.
더 흥미롭게도, 허브 제품은 parent drug and metabolites의 수송체 및 대사 효소 매개 PK 특성에 영향을 미칠 수 있습니다.
홍경천 을 losartan과 병용 투여 했을 때 R. rosea 는 CYP2C9 및 P-gp 억제로 인해 losartan의 혈장 농도를 증가시켜 losartan의 생체이용률을 증가시켰습니다.
흥미롭게도, 로자탄의 활성 대사산물인 EXP-3174의 혈장 농도는 R. rosea 에 의한 CYP2C9 억제로 인해 losartan으로부터의 EXP-3174 형성이 감소되었음에도 불구하고 증가했습니다 .
이는 CYP2C9 매개 대사에 대한 R. rosea 의 억제 효과가 losartan보다 EXP-3174에서 더 강했기 때문일 수 있습니다.
장, 간 및 신장이 수송 체 및 대사 효소를 발현하는 주요 기관으로 알려져 있음을 고려할 때 , 장, 간 및 신장의 약초 제품으로 인한 약물의 수송 체 및 대사 효소 매개 PK 변화가 HDI 평가의 주요 초점이었습니다.
PK 기반 HDI 평가 및 해석의 문제
HDI 평가에서 다양한 결과와 HDI 결과에 대한 부적절한 해석의 원인으로 세 가지 이유가 제시된다.
이러한 이유는 다음과 같습니다.
(1) 허브 제품의 복잡한 특성;
(2) 다양한 분석 시스템(예: 시험관 내 및 생체 내)에 대한 약물 및/또는 허브 노출의 반응; 및
(3) 연구 설계의 다양한 요인(예: 용량, 치료 기간, 투여 경로 등) .
3.1. 허브 제품의 복잡한 특성
허브 제품은 단일 추출물 또는 여러 성분을 포함하는 복합 추출물로 사용됩니다.
동일한 학명을 가진 식물에서 추출한 허브 또는 허브 추출물의 화학 성분은 재배 지역, 수확 시기, 보관 조건 및 추출 방법에 따라 다를 수 있습니다. .
이러한 이유로 유사하거나 동일한 화학 조성을 가진 한약 추출물 또는 한약 제제를 제조하는 것이 쉽지 않습니다.
즉, HDI 평가에서 다른 연구 그룹에서 사용하는 한약 추출물의 품질 차이가 다를 수 있습니다.
따라서 동일한 이명을 가진 식물 재료로 만든 약초 제제를 사용한 HDI 평가는 상충되는 결과로 끝날 수 있습니다.
불순물, 오인, 오염 또는 대체를 포함하여 허브 제제의 특성에 대한 기타 변경 사항도 발생할 수 있습니다. .
더욱이, 한방 제품에는 다양한 생리 활성 화합물이 포함되어 있으므로 순수한 활성 성분을 기반으로 한 HDI 연구 결과는 한방 제품 자체(즉, 한방 추출물)를 탐색하여 얻은 HDI 결과와 일치하지 않을 수 있습니다.
예를 들어, 생약 제품의 알려지지 않은 성분은 사이토크롬 P450(CYP)을 조절할 수 있지만 그 양과 CYP에 대한 억제/유도 효능은 예측할 수 없습니다. .
따라서 HDI 결과를 보고할 때 한약재 제제에 사용된 식물의 이명 및 부분, 추출 방법 및 한약재 제제의 화학적 조성(예: 다르게 제조된 배치 간의 화학적 및 생체 반응 지문)을 제공해야 합니다.
3.2. 다양한 분석 시스템에 대한 약물 또는 허브 제품의 노출 반응
다양한 분석 시스템(예: 시험관 내 또는 생체 내 전임상 및 임상 연구)에 대한 약물 및/또는 생약 제품의 노출에서 일관되지 않은 반응이 발생할 수 있습니다.
한약재가 대사 경로에만 영향을 미치고 이 대사 경로가 병용 약물의 처분에서 일차적인 특성인 경우, 시험관 내 대사 연구는 인간에게 시험관 내 데이터를 추론하여 임상 HDI를 예측하는 데 중요합니다.
위에서 언급한 많은 시험관 내 시스템이 HDI를 예측하는 데 효과적으로 사용되었지만, 시험관 내 분석 시스템은 때때로 PK 기반 HDI를 유발하는 기본 메커니즘을 설명하는 본질적인 단점을 보여, 다양한 시험관 내 분석을 사용하는 HDI 평가의 도전적인 문제를 보여줍니다.
대사 상호 작용을 평가하기 위해 시험관 내 분석 시스템에서 널리 사용되는 간 마이크로솜은 소포체에 국한된 효소만이 간 마이크로솜에 포함되어 있고 다른 효소를 통한 대사 상호 작용을 감지할 수 없기 때문에 실제 생체 내 상황을 나타내지 않습니다.
운반체와 대사 효소를 통한 동시 상호 작용은 생체 내 ADME 과정에 관여하므로 시험관 내 스크리닝에서 하나의 표적 대사 효소 또는 운반체는 충분하지 않으며 생체 내 현상과 관련이 없습니다.
더욱이, 경구 투여된 진세노사이드는 간 CYP에 영향을 미치고, 그 대사산물은 생체 내에서 장내 P-gp도 변경합니다.
그러나, 진세노사이드와 그 대사산물이 대사 효소 또는 수송체 매개 상호작용에 미치는 영향은 시험관 내 분석 시스템에서 동시에 조사할 수 없습니다.
따라서 생체 내 전임상 시스템은 약초 제품 및 약물의 성향을 고려하여 HDI 결과를 평가하는 데 필요합니다(즉, 약물 성향에 영향을 미치는 허브 제품에 의한 대사 효소 및 수송체의 동시 조절).
영장류와 설치류 사이의 종간 다양성으로 인해 생체 내 전임상과 임상 결과 사이에 상충되는 결과가 여전히 존재합니다.
예를 들어, 대사 효소 및 P-gp ,신장 유기 음이온 수송기 (OATs) 및 유기 양이온 수송기 (OCTs) 와 같은 수송기의 종간 다양성은 모순되는 HDI 결과 에 기여할 수 있습니다.
또한, 생체 내 전임상 연구의 용량 및/또는 치료 기간이 임상적으로 권장되는 용량 요법을 반영하지 않는 경우가 있으므로 생체 내 전임상 및 임상 데이터 간의 용량 요법의 추론을 고려해야 합니다.
또한 다양한 분석 시스템에서 HDI의 결과는 허브 추출물의 여러 구성 요소의 결과로 변동될 수 있습니다
허브 추출물의 여러 구성 요소는 특정 대사 효소 및 운반체와 개별적으로 상호 작용하거나 상호 작용하지 않을 수 있으며, 이는 공동 투여되는 약물의 약동학 변화에도 영향을 미칠 수 있습니다.
경구 투여된 생약 추출물의 흡수되지 않은 성분은 동시 투여된 약물의 간 대사에서 생체 내 상호 작용에 관여하지 않습니다 .
그러나, 한약 추출물의 모든 성분, 심지어 생체 내 흡수 부족으로 간에 도달하지 못하는 일부 구성 성분은 간세포와 간 마이크로솜을 사용하여 시험관 내 시스템에서 약물과 함께 치료됩니다.
따라서 시험관 내 시스템과 생체 내 시스템 간에 일치하지 않는 HDI 데이터가 발생할 수 있습니다.
3.3. 연구 설계의 다면적 요인(예: 투여 경로, 용량, 치료 기간 등)
투여경로, 용량, 치료기간, 탐지물질(probe chemicals=기질, 억제제, 유도물질 등)은 HDI의 발생 여부를 결정짓는 중요한 요소로, HDI 검사 결과가 일관되지 않을 수 있다.
따라서 HDI 연구의 결과를 설명할 때 다양한 요인을 정교하게 추정하고 고려해야 한다( 그림 2 및 표 1 ).
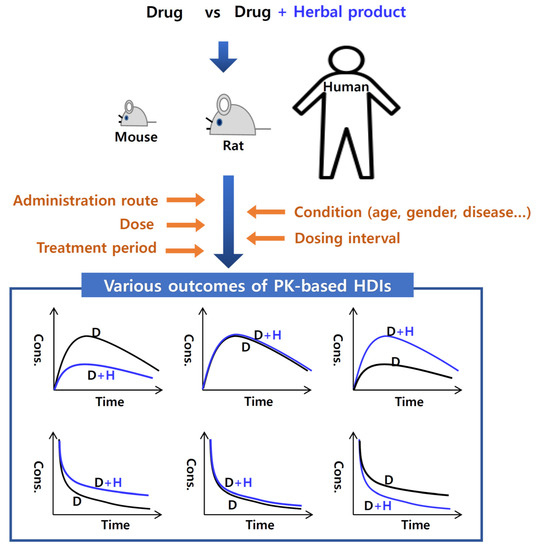
그림 2. 허브-약물 상호작용(HDI) 및 약동학(PK) 상호작용의 잠재적 결과에 영향을 미치는 요인의 개략도.
위의 3개의 그래프는 약초 제품이 있거나 없는 경우, 약물의 경구 투여 후 약물의 혈장 농도-시간 곡선을 나타냅니다.
왼쪽, 공동-투여된 한약 제품은 약물의 혈장 농도를 감소시키고;
가운데; 함께 투여되는 허브 제품은 약물의 혈장 농도에 영향을 미치지 않습니다.
오른쪽; 함께 투여된 허브 제품은 약물의 혈장 농도를 증가시킵니다.
또한 아래 3개의 그래프는 약초 제품이 있거나 없는 겨우,약물의 정맥내 투여 후 약물의 혈장 농도-시간 곡선을 나타냅니다.
왼쪽, 공동-투여된 한약 제품은 약물의 혈장 농도를 증가시키고;
가운데; 함께 투여되는 허브 제품은 약물의 혈장 농도에 영향을 미치지 않습니다.
오른쪽; 함께 투여되는 허브 제품은 약물의 혈장 농도를 감소시킵니다.
모든 경우에 허브 제품은 경구 투여됩니다.
D와 H는 각각 약품과 한약재를 나타낸다.
표 1. 상충되는 HDI 결과를 일으키는 요인.
Table 1. Factors causing conflicting HDI outcomes.
| Administration route | Ginkgo biloba leaf extract (oral, p.o.) | G. biloba leaf extract only alters the PK of orally, but not intravenously, administered nifedipine in rats | Due to inhibition of CYP3A in intestine, not in liver | [61] |
| Zingiber officinale root juice (p.o.) | Z. officinale juice decreases the oral bioavailability of cyclosporine, but the PK property of intravenous cyclosporine is not altered in rats | Due to inhibition of CYP3A and P-gp in intestine, not in liver | [62] | |
| Echinacea purpurea root (p.o.) | E. purpurea root extract reduced systemic clearance of midazolam following intravenous administration, but oral clearance of midazolam was not altered in rats | Due to inhibition of CYP3A in liver, not in intestine | [77] | |
| Ginseng berry extract (p.o.) | Ginseng berry extract did not affect the PK properties of intravenous administered nifedipine or cyclosporin, but markedly increased the absolute bioavailability of both drugs after oral administration in rats | Due to inhibition of CYP3A in intestine, not in liver | [77] | |
| Schisandra chinensis fruit (p.o.) | S. chinensis fruit extract increased AUC and Cmax of orally administered midazolam, but there was no little change in the PK properties of intravenously administered midazolam in rats | Due to intensive inhibitory effect on CYP3A in intestine, not in liver | [64] | |
| Dose | Andrographis paniculata extract (p.o.) | Low dose of Andrographis Herba extract increases theophylline elimination, whereas high-dose of A. paniculata extract decreases theophylline elimination | Due to induction of CYP1A2 by low-dose treatment of A. paniculata extract, but inhibition of CYP1A2 by its high-dose treatment | [72] |
| Tinospora cordifolia aqueous-alcoholic extract (p.o.) | High-dose of T. cordifolia aqueous-alcoholic extract, not low-dose, reduced the clearance and increased bioavailability of glibenclamide, respectively, in rats | Due to the inhibition of CYP2C9, 2D6 and 3A4 in liver by high-dose of T. cordifolia aqua-alcoholic extract, not low-dose | [73] | |
| Treatment period | S. chinensis fruit extract (p.o.) | Long-term treatment of S. chinensis fruit extract reduced AUC and Cmax of orally administered midazolam, but the AUC and Cmax of orally administered midazolam were increased after single treatment of Schisandrae Chinensis Fructus extract | Due to stronger induction of CYP3A in liver and intestine than inhibition of CYP3A in long-term treatment; Due to stronger inhibition of CYP3A in intestine, not in liver after single treatment |
[72] |
| G. biloba leaf extract (p.o.) | Single treatment of G. biloba leaf extract increased the intravenously administered diltiazem concentrations in plasma, but long-term treatment of ginkgo biloba leaf extract reduced the intravenously administered diltiazem concentrations in plasma | Due to inhibition of CYP3A in liver in singe treatment of G. biloba leaf extract; due to induction of CYP3A in liver after long-term treatment | [68,76] | |
| Lonicera japonica extract (p.o.) | 28-day treatment of L. japonica extract increased metformin concentration in liver along with the enhancement of glucose tolerance activity of metformin, but single and 7-day treatment of Lonicera japonica extract did not alter metformin concentration in plasma and liver as well as glucose tolerance activity. | Due to reduction in mate1-mediated biliary excretion of metformin by 28-day treatment of Lonicera japonica extract | [29] | |
| Houttuynia cordata extract (p.o.) | 28-day treatment of H. cordata extract increased metformin concentration in plasma, liver and kidneys along with the enhancement of glucose-lowering effect in rats, but there no change of PK and PD of metformin after single and 7-day treatment of Houttuynia cordata extract | Increase in metformin plasma concentrations due to the decrease in renal oct2-mediated renal excretion of metformin and metformin concentration in kidneys; enhancement of glucose tolerance activity due to the increase in oct1-mediated renal uptake of metformin | [30] |
표 1. 상충되는 HDI 결과를 일으키는 요인.요인허브 제품HDI 결과PK 기반 HDI 메커니즘참조
| 관리 경로 | 은행잎 추출물 (경구, 포) | G. 빌로바 잎 추출물은 쥐에게 니페디핀을 경구 투여한 경우에만 약동학(PK)을 변화시켰지만 정맥내 투여하지 않았습니다. | 간이 아닌 장에서 CYP3A의 억제로 인해 | [61] |
| Zingiber officinale 뿌리 주스 (po) | Z. officinale 주스는 사이클로스포린의 경구 생체이용률을 감소시키지만 정맥내 사이클로스포린의 PK 특성은 쥐에서 변경되지 않습니다 | 간이 아닌 장에서 CYP3A 및 P-gp의 억제로 인해 | [62] | |
| Echinacea purpurea 뿌리 (po) | E. purpurea 뿌리 추출물은 정맥 투여 후 midazolam의 전신 청소율을 감소시켰지만, midazolam의 경구 청소율은 쥐에서 변하지 않았습니다. | 장이 아닌 간에서 CYP3A의 억제로 인해 | [77] | |
| 인삼열매추출물(포) | 인삼베리 추출물은 니페디핀 또는 사이클로스포린을 정맥 투여한 경우 약동학 특성에 영향을 미치지 않았지만 쥐에게 경구 투여한 후 두 약물의 절대 생체이용률을 현저히 증가시켰습니다. | 간이 아닌 장에서 CYP3A의 억제로 인해 | [77] | |
| 오미자 열매(포) | S. chinensis 과일 추출물은 경구 투여된 midazolam의 AUC와 Cmax를 증가시켰으나, 쥐에서 정맥 투여된 midazolam의 약동학 특성에는 거의 변화가 없었습니다. | 간이 아닌 장에서 CYP3A에 대한 집중 억제 효과로 인해 | [64] | |
| 정량 | 안드로그라피스 파니쿨라타 추출물(포) | Andrographis Herba 추출물의 낮은 복용량은 테오필린 제거를 증가시키는 반면, A. paniculata 추출물 의 고용량은 테오필린 제거를 감소시킵니다. | A. paniculata 추출물 의 저용량 처리에 의해 CYP1A2가 유도 되지만 고용량 처리에 의해 CYP1A2가 억제됨 | [72] |
| Tinospora cordifolia 수성 알코올 추출물 (po) | 저용량이 아닌 고용량의 T. cordifolia 수성 알코올 추출물은 쥐에서 각각 글리벤클라미드의 제거율을 감소시키고 생체이용률을 증가시켰습니다. | 저용량이 아닌 고용량의 T. cordifolia 아쿠아 알코올 추출물 에 의한 간에서의 CYP2C9, 2D6 및 3A4 억제로 인해 | [73] | |
| 치료기간 | S. chinensis 과일 추출물 (po) | 오미자추출물 의 장기투여는 midazolam 경구투여의 AUC와 Cmax를 감소시켰으나, 오미자추출물의 단독투여 후 경구투여 midazolam의 AUC와 Cmax는 증가하였다. | 장기 치료에서 CYP3A를 억제하는 것보다 간과 장에서 CYP3A가 더 강력하게 유도되기 때문입니다. 단일 치료 후 간이 아닌 장에서 CYP3A의 더 강력한 억제로 인해 |
[72] |
| G. 빌로바 잎 추출물(포) | G. biloba 잎 추출물 의 단일 치료는 혈장 내 정맥 투여된 딜티아젬 농도를 증가시켰지만, 은행나무 잎 추출물의 장기간 치료는 혈장 내 정맥내 투여된 딜티아젬 농도를 감소시켰습니다. | G. biloba 잎 추출물 의 단일 처리에서 간에서 CYP3A의 억제로 인해 ; 장기간 치료 후 간에서 CYP3A 유도로 인해 | [68,76] | |
| 로니케라 자포니카 추출물(포) | L. japonica 추출물 의 28일 처리는 메트포르민의 내당 활성 증진과 함께 간의 메트포르민 농도를 증가시켰지만, 로니케라 추출물의 단일 및 7일 처리는 내당 뿐 아니라 혈장 및 간의 메트포르민 농도를 변화시키지 않았다. 활동. | 자포니카 추출물 28일 처리에 의한 mate1 매개 담즙 배설 감소로 인한 메트포르민 | [29] | |
| Houttuynia cordata 추출물(포) | 쑥 추출물 의 28일 처리는 혈장, 간 및 신장의 메트포르민 농도를 증가시켰고 쥐의 혈당 강하 효과를 향상시켰으나, 홍삼 단독 및 7일 처리 후 메트포르민 의 약동학 및 PD 변화는 없었습니다. 발췌 | 신장에서 메트포르민 및 메트포르민 농도의 신장 oct2 매개 신장 배설 감소로 인한 메트포르민 혈장 농도 증가; metformin의 oct1 매개 신장 흡수 증가로 인한 내당능 활성 향상 | [30] |
첫째, 한약재와 약물의 투여 경로를 고려해야 한다.
대부분의 생약 제품이 임상 사례에서 경구 투여된다는 점을 고려할 때, 특히 약물을 경구 투여하는 경우 장내 대사 매개 상호작용이 중요하다.
특히 장 부위의 HDI도 임상적으로 관련이 있으므로 신중하게 검사해야 합니다.
한약재와 약물 모두 대부분의 경우 경구 투여되고 많은 수의 대사 효소와 수송체가 장에서 발현되기 때문입니다.
예를 들어, 경구 투여된 은행나무 잎 추출물은 쥐에서 니페디핀이 경구 투여될 때만 약동학을 변경하지만 정맥내 투여는 아닙니다.
경구 투여 된 Zingiber officinale 뿌리 주스는 사이클로스포린의 경구 생체이용률을 감소시키지만 정맥내 사이클로스포린의 PK는 변경되지 않습니다.
이 현상은 간과 장의 대사 효소에 대한 허브의 조절 효과가 다르기 때문일 수 있습니다.
또한 오미자 열매 추출물은 간 CYP3A보다 장 CYP3A에 더 집중적으로 조절 효과를 나타냅니다.
둘째, 한약재와 약물의 투여량에 따라 HDI 결과가 다르게 나타난다.
허브 제품은 일반적으로 CYP에 대해 용량 의존적 유도 또는 억제 효과를 나타내며 흥미롭게도 때때로 CYP에 이상 효과를 나타낼 수 있습니다.
예를 들어, 유도는 낮은 복용량에서 발생하고 억제는 더 높은 복용량의 허브 제품에서 발생합니다.
낮은 용량의 Andrographis paniculata 추출물로 전처리하면 CYP1A2의 유도로 인해 테오필린 제거가 증가하는 반면, 고용량의 A. paniculata 는각각 CYP1A2의 억제로 인한 테오필린 제거를 감소시킨다.
쥐에서 Tinospora cordifolia 수성 알코올 추출물과 글리벤클라미드를 병용 투여하는 경우, 저용량(100mg/kg)이 아닌 고용량(400mg/kg) Tinospora cordifolia 수성 알코올 추출물만 투여한 경우, CYP 2C9, 2D6 및 3A4를 통한 제거 감소로 인해 글리벤클라미드의 경구 생체이용률 증가하였습니다..
셋째, 치료 기간이 HDI의 발생에 영향을 미칠 수 있습니다.
한방 제품을 사용한 장기 치료가 일반적이므로 대사 효소 및/또는 수송체에 대한 한약 제품의 효과는 일반적으로 치료 기간에 따라 다르게 나타납니다.
예를 들어, S. chinensis 과일 추출물을 사용한 단기 치료는 억제 효과를 나타내지만 장기 치료는 간 및 장 CYP3A 모두에 대한 유도 효과를 나타냅니다.
Glycyrrhiza glabra 뿌리 추출물 의 단일 용량은 마우스에서 CYP에 영향을 미치지 않지만, 반복 처리는 간 CYP3A를 유도하고, 2B1 및 1A2를 덜 유도합니다.
G. biloba 잎 추출물은 일반적으로 대부분의 병용 약물의 대사에 억제 효과를 나타내지만, 반대로 장기간 전처리하면 간 대사 활성이 유도됩니다.
또한 Han et al은 28일 동안 메트포르민과 자포니카 추출물을 동시에 처리한 쥐에서 mate1 매개 담즙 배설 감소로 간에서 메트포르민 농도가 증가했다고 보고한 바 있다.
단일 또는 7일 치료. 그들은 또한 28일의 치료 기간에서만 메트포르민의 내당능 활성의 향상을 관찰했습니다.
You et al. [30]은 메트포르민의 신장 oct2 매개 신장 배설 감소로 인해 메트포르민의 혈장 농도-시간 곡선(AUC) 면적이 증가했다고 보고했으며, 그리고 28일 동안 메트포르민과 홍삼 추출물을 병용 투여한 쥐에서 oct1 매개 신장 흡수와 함께 메트포르민의 혈당 강하 효과 증가로 인해 신장의 메트포르민 농도가 증가했습니다.
이러한 상호작용은 메트포르민과 H. cordata 추출물 을 단일 및 7일 동시 처리한 쥐에서는 발생하지 않았습니다 .
따라서 적절한 치료 기간을 선택하는 것이 HDI 평가에 중요합니다.
'약물' 카테고리의 다른 글
| 허브 약물 상호 작용에 대한 환자 상담 (0) | 2022.09.15 |
|---|---|
| 허브-약물 상호작용의 증거 및 메커니즘 개요 (1) | 2022.09.15 |
| 약물 상호 작용의 일반 원칙 (0) | 2022.09.15 |
| 임상 증상을 기반으로 한 허브 및 기존 약물 상호 작용의 현재 관점 (0) | 2022.09.14 |
| 허브-약물 상호 작용: 메커니즘 및 임상 측면의 개요 (0) | 2022.09.14 |