2016
https://koreascience.kr/article/JAKO201614139533171.1ff8page
The Role of Resveratrol in Lipid Metabolism: A Systematic Review of Current Basic and Translational Evidence -Journal of Foo
Abstract Resveratrol is a non-flavonoid polyphenol which belongs to the stilbenes group and is naturally generated in several plants in response to damage or fungal invasion. It has been shown in published studies that resveratrol has an anti-adipogenic ef
koreascience.kr
The Role of Resveratrol in Lipid Metabolism: A Systematic Review of Current Basic and Translational Evidence
in vitro 연구에서 레스베라트롤은 지방생성을 줄여주고 apoptosis를 증가시켜 지방세포의 발달과정에 기인하며, 지방세포의 분화에 있어 중요한 전사인자인 C/EBPβ, C/EBPα, SREBP1c 및 PPARγ의 활성을 감소시켜 항 비만 효과를 유발하는 효과가 있다는 것이 많은 논문들을 통해 증명되었다.
또한, in vivo 연구에서 레스베라트롤은 지방 축적 과정을 억제하고 지질 분해 및 산화 경로를 자극하여 체지방 증가율을 감소시킨다는 것이 증명되었다.
최근 다양한 연구의 결과물(Table 2)들은 레스베라트롤이 지방생성, 지방분해, 열발생 및 지방산 산화에 관여하며 또한, 백색 지방을 갈색 지방으로 변화시키는 능력이 있다는 것을 증명하였다.
하지만 인간에 대한 레스베라트롤의 명확한 메커니즘을 알지 못하고 인간에게 나타나는 부작용에 관한 연구가 없기 때문에, 안전성을 확보하기 위해서는 다양한 실험모델을 이용한 레스베라트롤의 단기간 및 장기간에 대한 깊은 연구가 요구된다.
http://foodsafety.or.kr/journal/article.php?code=39717
:: Journal of Food Hygiene and Safety ::
레스베라트롤(trans-3,4',5-trihydroxystilbene) (Fig. 1)은 스 틸벤(stilbene)과에 속해있으며 몇몇 식물에서 상처나 균에 반응하여 자연적으로 생겨나는 비-플라보노이드 폴리페놀 이다1). 레스베라트롤은
foodsafety.or.kr
또한, 백색 지방 조직에서 트리아실글리세롤 대사에 관여하는 다양한 대사 경로가 레스베라트롤에 의해 조절되는 것으로 나타났습니다.
지방분해와 관련하여 이 화합물 자체는 지방분해를 일으키지 않는 것처럼 보이지만 β-아드레날린 작용제에 의해 자극되는 지질 동원을 증가시킵니다.
갈색 지방 조직의 열 생성 증가 및 그에 따른 관련 에너지 소산, 레스베라트롤의 체지방 감소 효과를 설명할 수 있습니다.
레스베라트롤은 지방 조직에 미치는 영향 외에도 다른 기관과 조직에도 작용할 수 있습니다.
따라서 미토콘드리아 생합성을 증가시켜 골격근과 간에서 지방산 산화를 증가시킵니다.
이 효과는 또한 이 분자의 체지방 감소 효과에 기인할 수 있습니다.
**********************************************************************
2011
https://www.cell.com/cell-metabolism/pdf/S1550-4131(11)00386-X.pdf
레스베라트롤은 에너지 대사와 미토콘드리아 기능에 영향을 미치는 천연 화합물이며 적어도 비만 동물 모델에서 칼로리 제한 모방체 역할을 합니다.
여기에서 우리는 30일 동안 무작위 이중 맹검 교차 연구에서 11명의 건강한 비만 남성을 위약과 150mg/day 레스베라트롤(resVida)로 치료했습니다.
레스베라트롤은 수면 및 휴식 대사율을 현저히 감소시켰습니다.
근육에서 레스베라트롤은 AMPK를 활성화하고, SIRT1 및 PGC-1a 단백질 수준을 증가시키고, 미토콘드리아 함량의 변화 없이 시트레이트 합성효소 활성을 증가시키고, 지방산 유래 기질에 대한 근육 미토콘드리아 호흡을 개선했습니다.
또한 레스베라트롤은 근육 세포 내 지질 수준을 높이고
간내 지질 함량 감소, 순환 포도당, 트리글리세리드, 알라닌-아미노트랜스퍼라제 및 염증 마커.
레스베라트롤 투여 후 수축기 혈압이 떨어지고 HOMA 지수가 개선되었습니다.
식후 상태에서는 지방조직의 지방분해와 혈장지방산과 글리세롤이 감소하였다.
결론적으로, 우리는 30일간의 레스베라트롤 보충이 칼로리 제한의 효과를 모방하여 비만인의 대사 변화를 유도한다는 것을 보여줍니다.
*************************************************************************************
2019
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6601040/
Resveratrol Action on Lipid Metabolism in Cancer
Cancer diseases have the leading position in human mortality nowadays. The age of oncologic patients is still decreasing, and the entire scientific society is eager for new ways to fight against cancer. One of the most discussed issues is prevention by ...
www.ncbi.nlm.nih.gov
Resveratrol Action on Lipid Metabolism in Cancer
지방산(FA) 합성은 중심 대사 전구체인 아세틸-CoA의 생성을 통해 포도당에 크게 의존합니다.
종양 세포에서 대부분의 지방 FA는 지방산 합성 효소(FASN)에 의해 새로 합성되어 집중적인 생체 에너지와 구조적 변화를 조정합니다.
실제로 FASN은 종양학에서 세포 증식의 마커이자 약물 표적으로 정의되었습니다
혈장 내 총 콜레스테롤의 증가는 종양의 발달을 가속화할 수 있고 질병의 공격성과 관련이 있습니다.
1. 레스베라트롤과 지방산 합성
암에서 동화작용과 이화작용을 모두 포함하는 FA 대사의 역할은 최근 몇 년 동안 점점 더 주목을 받고 있습니다.
지질 합성에는 영양소에서 파생된 탄소를 FA로 전환하는 과정이 포함됩니다.
건강한 성인에서 새로운 FA 생합성은 간, 지방 조직, 수유 중인 유방 조직또는 뇌에서 발생합니다.
그러나 암세포에서 FA는 TAG 저장을 사용하기보다 막 지질 합성을 위해 인지질(PL)로 에스테르화되어 세포 복제를 촉진합니다.
실제로, 암세포에서 FASN을 차단하면 세포 성장이 정지되고 세포 사멸이 유도되는 것으로 나타났습니다.
RES는 많은 암 세포주에서 FASN의 하향 조절을 통해 지질 합성을 유의하게 감소시켰습니다.
Table 1
Main molecular mechanisms involved in resveratrol action regarding lipid metabolism in cancer.
| FASN | Breast cancer | SKBR-3 | 5–150 µM (IC50 ~ 80 µM) |
• decrease in FASN and Her2 expression in a dose-dependent manner | [86] |
| Pancreatic cancer | MIA PaCa-2 | 50 and 100 µM | • cell growth arrest via significant decrease in glycogen breakdown and glucose carbon redistribution toward FAs by reducing FASN | [83] | |
| SIRTUIN | Colorectal cancer | HCT116 SW480 |
1, 5, 10, 20, and 50 µM | • stimulation of the expression of SIRT1 in a dose-dependent manner • downregulation of nuclear localization of NF-κB, NF-κB phosphorylation and its acetylation, causing attenuation of NF-κB-regulated gene products involved in tumor invasion and metastasis |
[124] |
| Breast cancer | MCF7 MDA-MB-231 |
10, 25, and 50 µM |
• decrease in breast cancer cell mass and viability in a dose-dependent manner • increase in SIRT1 and SIRT3 protein content |
[123] | |
| Hepatocellular carcinoma | HepG2 Bel-7402 SMMC-7721 |
20–200 µmol/L | • inhibition of cell viability and proliferation and increase in apoptosis in a dose-dependent manner • activation of SIRT1 and inhibition of SIRT1-mediated post-translational modification of PI3K/AKT signaling |
[91] | |
| Glioblastoma | GSCs derived from human biopsies | 0–300 µM | • alteration of cell morphology after RES in the doses above 150 µM induction of GSCs necrosis • no effect on NSCs • blockade of SIRT2 activity or downregulation of SIRT2 expression with siRNAs counteracted the inhibitory effect of RES on cell proliferation |
[125] | |
| Chondrosarcoma cancer |
JJ012 | 5, 10, 25, 50, 100, and 200 µM | • increase in the protein expression of SIRT1 in a dose-dependent manner • significant reduction of the acetylation of NF-κB-p65 in a time-dependent manner (dose 50 μM) |
[141] | |
| BALB/cA-nu (nu/nu) mice | 50 or 100 mg/kg body weight | • reduction in size and weight of JJ012 tumors • reduction in tumor growth without affecting the body weight of the mice • increase in SIRT1 and cleaved caspase-3 expressions |
[141] | ||
| SREBP | Prostate cancer | MiaPaCa-2 Panc-1 | 50 and 100 mmol/L | • inhibition of lipid synthesis via SREBP1 • enhancing the sensitivity of gemcitabine • reversed the gemcitabine-induced stemness |
[100] |
| LSL- KrasG12D/+ Trp53fl/+ Pdx1-Cre (KPC) |
50 mg/kg body weight | • decrease in SREBP1 expression in tumor tissues • decrease in expression levels of the stem cell markers • decrease in PCNA protein synthesis |
[100] | ||
| Breast cancer | female nude mice | 22.4 mg/kg body weight |
• suppression of DCIS formation • reduction of tumor volume reduction in lipid content in serum • inhibition of SREBP1 and its downstream genes ACLY, ACC1, and FAS |
[101] | |
| DCIS.com | 50 and 100 µM | • suppression of CSCs growth • decrease in cell proliferation in CSCs in a dose-dependent manner • reduction of lipid content • inhibition of protein and mRNA level of SREBP1 and its downstream lipogenic genes • inhibition of mammosphere formation by CSCs |
[101] | ||
| Liver cancer | HepG2 | 15, 45, or 135 μmol/L | • reduction of intracellular lipid droplets • attenuation of hepatic steatosis • decrease of levels of intracellular TAGs enhancement of the phosphorylation of AMPK and downregulation of SREBP-1c and lipin 1 |
[142] | |
| PI3K/AKT/mTOR | Colon cancer | HCT116 | 10–80 µM | • inactivation of PI3K/AKT signaling via upregulation of bone morphogenetic protein BMP7 • decrease of the growth of cancer cells in a dose- and time-dependent manner |
[93] |
| Breast cancer | SKBR-3 | 20, 40, and 60 µM | • inhibition of AKT phosphorylation • alteration of AKT/PI3K/mTOR pathway |
[86] | |
| Hepatocellular carcinoma | HepG2 Bel-7402 SMMC-7721 |
20–200 µmol/L | • inhibition of cell viability and proliferation • increase in apoptosis in a dose-dependent manner • activation of SIRT1 and inhibition of SIRT1-mediated post-translational modification of PI3K/AKT signaling |
[91] | |
| Gastric cancer | MGC803 | 6.25, 12.5, 25, 50, 100, 200, and 400 μM | • decrease in protein levels of p-PI3K and p-AKT in a dose-dependent manner • decrease in protein level of p-PTEN (inactive) in a dose-dependent manner • cell growth inhibition in a dose- and time-dependent manner • cell cycle arrested in G0/G1 phase |
[92] | |
| Glioblastoma | U87 GSCs isolated from the patients BALB/c nude mice |
0–100 µM 100 μg/mL |
• deactivating oncogenic AKT and activating the tumor suppressor p53 gene network • inhibition of glioma cells and GSCs self-renewal and proliferation • reduction of tumor growth |
[143] | |
| GSCs isolated from the patients | 5, 10, and 20 µM | • inhibition of the invasion of GSCs via downregulation of the PI3K/AKT/NF-κB signaling pathway | [85] | ||
| NOD/SCID mice | 10 mg/kg body weight | • decrease in GSCs adhesion in a dose-dependent manner • suppression of GSCs adhesion in vivo |
[85] |
CSCs—cancer stem cells; DCIS—ductal carcinoma in situ; FASN—fatty acid synthase; GSCs—glioblastoma stem cells; NSCs—neuronal stem cells; SIRTUIN—silent mating type information regulation; SREBP—sterol regulatory element-binding protein; PCNA—proliferating cell nuclear antigen; PI3K/AKT/mTOR—phosphoinositide-3-kinase/protein kinase B/mammalian target of rapamycin.
FA 및 콜레스테롤 생합성에 관여하는 많은 유전자의 발현은 phosphoinositide-3-kinase/protein kinase B/mammalian target of rapamyci(PI3K/AKT/mTOR) 경로를 통해 활성화됩니다.
RES는 PI3K/AKT/mTOR 경로를 비활성화하여 다양한 암세포의 성장을 용량 의존적으로 감소시킬 수 있는 것으로 나타났습니다.
예를 들어, 환자로부터 분리된 교모세포종 시작 암 세포에서 5, 10 및 20μM 용량의 RES는 시험관 내 및 생체 내에서 PI3K/AKT/NF-κB 신호 전달 경로의 하향 조절을 통해 이러한 세포의 침입을 억제했습니다.
2. 레스베라트롤과 콜레스테롤 경로
막 기능에 중요한 지질의 또 다른 부류는 스테롤, 주로 콜레스테롤 및 콜레스테릴-에스테르입니다.
콜레스테롤은 에스트로겐 및 프로게스테론과 같은 스테로이드 호르몬 합성을 위한 구조적 백본을 제공합니다
스테롤 조절 요소 결합 단백질(SREBP) 계열은 FA 및 콜레스테롤 생합성에 관여합니다.
비정상적으로 상승된 콜레스테롤 수치는 3-hydroxy-3-methyl glutaryl coenzyme A reductase(HMGCR)에 의해 매개되는 SREBP에 기인할 수 있습니다.
RES는 메발로네이트 경로를 억제하고, HMGCR 발현과 활성을 감소시키고, 쥐의 테카-간질 세포에서 콜레스테롤 합성을 감소시켰다.
또한, 50 μmol/L의 용량에서 MiaPaCa-2 및 Panc-1 췌장암 세포와 50 mg/L 용량의 췌장암 형질전환 마우스 모델에서 SREBP1 억제를 통해 지질 합성을 억제하는 것으로 밝혀졌습니다.
3. 레스베라트롤, 세라마이드 및 아라키돈산 경로
임상시험
인간 연구에서 RES의 주요 문제는 낮은 생체 이용률과 설사, 메스꺼움, 헛배부름 및 복부 불편을 포함한 경미한 위장 불편의 형태로 가능한 부작용입니다.
결론
전임상 및 임상 증거는 지질 대사가 종양 발달 및 침윤에 중요한 역할을 한다는 것을 분명히 보여줍니다.
지질 대사에 참여하는 수많은 단백질은 암세포의 생존과 증식에도 관여합니다.
많은 약물과 천연 화합물이 지질 대사를 조절하여 발암 과정에 영향을 미치는 능력으로 인해 연구되고 있습니다.
RES는 지질 대사에 약간의 조절 효과를 나타내는 잘 알려진 천연 물질입니다.
RES는 다양한 메커니즘을 통해 암의 지질 대사를 변경하고 유기체의 요구와 관련하여 최적의 대사 정도에 기여합니다.
RES는 SREBP 억제를 통해 지질 합성을 억제하고, AMPK의 활성화와 동시에 시르투인을 활성화하고, PI3K/AKT/mTOR 경로를 하향 조절하여 암 세포 사멸을 초래합니다.
RES는 암 환자의 혈청 TAG, VLDL 및 LDL 수준을 감소시켜 종양 부피와 전이를 감소시킵니다.
따라서 암 발병 및 진행을 조절하는 데 사용할 수 있습니다.
******************************************************************************
2017
https://www.nature.com/articles/s41598-017-07006-0
Resveratrol reverses the Warburg effect by targeting the pyruvate dehydrogenase complex in colon cancer cells - Scientific Repor
Resveratrol (RES), a polyphenol found in natural foods, displays anti-oxidant, anti-inflammatory and anti-proliferative properties potentially beneficial in cancers, in particular in the prevention of tumor growth. However, the rapid metabolism of resverat
www.nature.com
Resveratrol reverses the Warburg effect by targeting the pyruvate dehydrogenase complex in colon cancer cells
레스베라트롤의 빠른 대사는 생체 이용률을 크게 제한합니다.
저용량 레스베라트롤의 잠재적인 생물학적 활성을 유지하는 분자 메커니즘은 광범위하게 연구되지 않았으므로 더 나은 특성화가 필요합니다.
여기에서 우리는 레스베라트롤(10 μM, 48 시간)이 결장암 세포에서 세포 성장 정지와 대사 재프로그래밍을 모두 유도한다는 것을 보여줍니다.
레스베라트롤은 오탄당 인산 활성 감소 및 ATP 생성 증가와 관련하여 지질 프로필을 수정하고 산화 능력을 증가시키며 해당 과정을 감소시킵니다.
레스베라트롤은 pyruvate dehydrogenase(PDH) 복합체를 표적으로 하며, 에너지 대사의 핵심 미토콘드리아 게이트키퍼로서 PDH 활성을 향상시킵니다.
칼슘 킬레이트화와 미토콘드리아 칼슘 유니포트의 차단은 레스베라트롤에 의한 산화 능력 증가와 PDH 활성 증가를 방지하여 칼슘이 대사 변화에 역할을 할 수 있음을 시사합니다.
******************************************************************************
2019
https://www.sciencedirect.com/science/article/pii/S0753332219310509
Resveratrol shifts energy metabolism to increase lipid oxidation in healthy old mice
The objective of this work was to determine the specific mechanisms by which resveratrol inhibits lipogenesis and stimulates lipolysis.Twelve male mic…
www.sciencedirect.com
Resveratrol shifts energy metabolism to increase lipid oxidation in healthy old mice
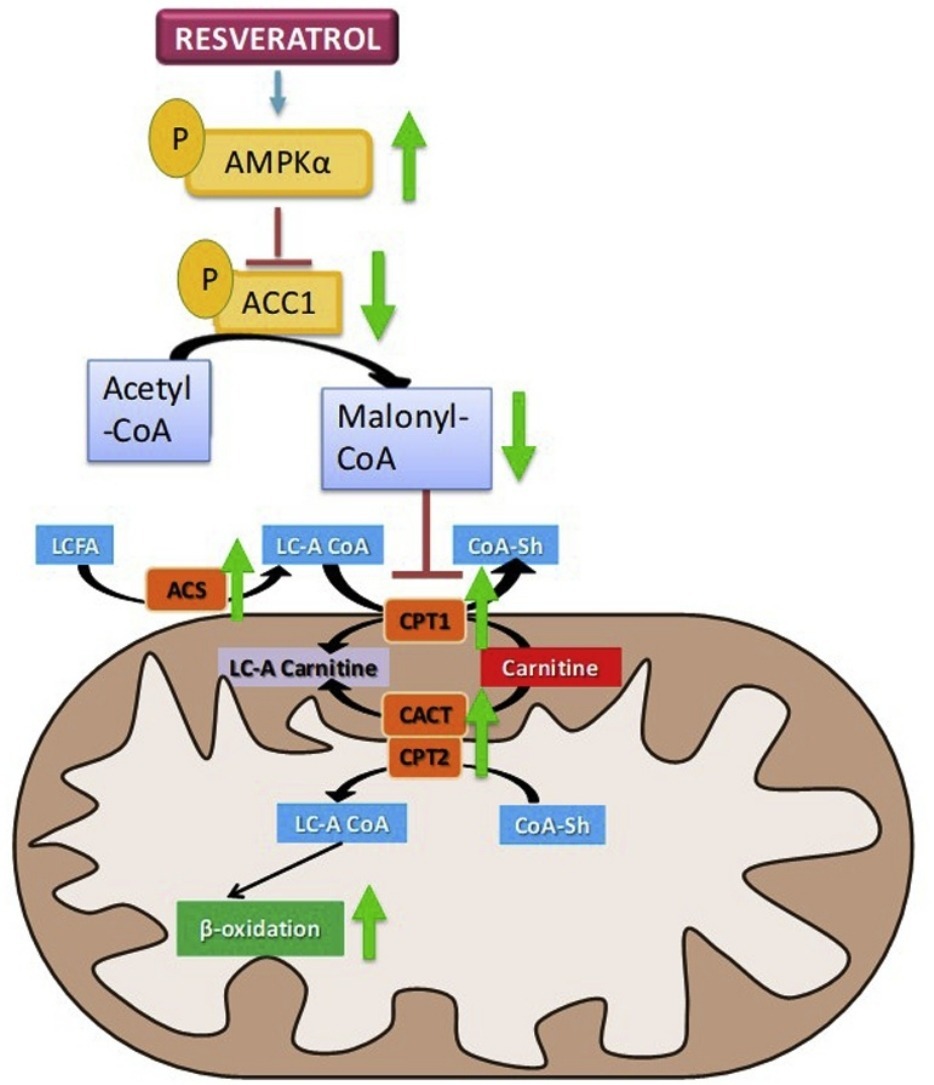
생체 내에서 레스베라트롤 이 간, 근육 및 지방 조직에서 AMPKα의 발현 및 인산화를 증가시키고 지질 이화작용에 관여하는 효소.인 아실-CoA 합성효소, 카르니틴 팔미토일 트랜스퍼라제 1 및 카르니틴 아실카르니틴 트랜스로카제의 발현을 증가시키는 것을 관찰했습니다.
다른 한편으로, 아세틸-CoA 카르복실라제의 수준과 그 산물인 말로닐 CoA의 수준이 감소합니다.
결론
우리는 조절된 용량의 레스베라트롤이 지방산 동원 및 분해를 활성화하고 늙은 쥐에서 지방산 합성을 억제한다고 결론지었습니다.
****************************************************************************
2014
https://erc.bioscientifica.com/view/journals/erc/21/3/R209.xml
Resveratrol and cancer: focus on in vivo evidence
동물에서 레스베라트롤의 추가 용량은 고지방식이의 많은 해로운 영향으로부터 보호하고 추가적인 건강상의 이점을 제공합니다.
부분적으로 trans -resveratrol의 낮은 생체 이용률 문제입니다
Wenzel & Somoza(2005) 는 레스베라트롤의 생체이용률과 대사에 대한 중요하고 상세한 검토를 제공합니다.
설치류와 인간에서 레스베라트롤을 경구로 섭취하면 70-80%가 내장에서 수동 확산을 통해 빠르게 흡수됩니다.
흡수 후, 레스베라트롤은 글루쿠로나이드와 황산염으로 결합되어 트랜스 -레스베라트롤의 순환 수준은 경구 투여 후 30-60분에 정점에 도달합니다.
인간에서, 변형되지 않은 트랜스 -레스베라트롤의 순환 수준은 25mg/70kg 체중의 단일 투여 후 총 유리 레스베라트롤 및 접합체의 최고 혈청 농도의 ~2%에 불과합니다.
또 다른 보고서에 따르면 레스베라트롤의 최소 70%는 25mg의 단일 용량 후 흡수되고 레스베라트롤과 모든 대사 산물에 대한 최고 혈청 농도는 2μM(~490ng/ml)입니다.
여러 번 경구 투여(29일 동안 매일 5g)한 후, 트랜스 -레스베라트롤의 혈장 농도는 ~4μM( 4.29nmol/ml)만큼 높은 것으로 보고되었습니다.
그러나 이 고용량의 레스베라트롤은 위장 부작용과도 관련이 있다는 점에 유의해야 합니다.
흥미롭게도, 인간의 결장 조직에서 레스베라트롤과 그 대사산물인 레스베라트롤-3- O 의 수준-글루쿠로나이드는 0.5-1.0g의 레스베라트롤을 하루에 한 번 경구 복용했을 때 높은 농도(각각 674 및 86nmol/g)에서 발견되었습니다.
레스베라트롤의 결합이 빠르고 생체이용률이 낮기 때문에 암 예방 및 치료를 위한 레스베라트롤의 생체 내 사용은 불확실합니다.
따라서 이 검토의 의도는 생체 내 연구의 결과를 강조하는 것입니다.
임상 연구
암 예방 및 치료를 위한 효과적인 보충제로서 레스베라트롤에 대한 임상 증거는 부족합니다.
2009년에 암 진단을 받은 환자의 레스베라트롤 치료를 조사한 첫 번째 1상 임상 시험이 발표되었습니다( Nguyen et al . 2009 ).
결장직장암 환자( n =8)는 진단 당시와 매일 레스베라트롤(20 또는 80mg/일, n =2 및 1) 또는 포도 분말(80 또는 120 g/일, n= 3 및 2)) 투여 후 14일에 정상 및 암성 장 점막 샘플을 생검했습니다.
가장 중요한 효과는 저용량 포도 분말에서 관찰되었습니다. 이로 인해 저자들은 포도에서 발견되는 다른 화합물과 함께 레스베라트롤을 사용하여 Wnt 경로 신호를 감소시켜 결장암 발병 위험을 감소시킬 수 있지만 확립된 결장암에 대해서는 효과적이지 않을 수 있다고 결론지었습니다.
두 번째 임상 연구에서는 간 전이가 있는 대장암 환자에서 레스베라트롤 치료의 효과를 관찰했습니다(n = 9). 레스베라트롤 보충(10-21일 동안 매일 5g의 미세이온화된 레스베라트롤 SRT501, n = 6)은 암성 간 조직에서 절단된 카스파제-3의 발현을 증가시켰으며, 이는 위약 치료 대상자에 비해 암 세포의 세포자멸사 증가를 나타냅니다( n = 3) .
이 임상 시험에서 환자 표본 크기가 작았으며(각각 연구에 등록된 암 환자는 8명과 9명), 암치료에 대한 레스베라트롤의 효능에 대한 인간 데이터가 거의 없다는 사실을 강조하는 것이 중요합니다. .
몇 가지 다른 임상 연구는 건강한 피험자의 암 예방 및 암 위험 요인에 대한 레스베라트롤 보충제 및 예측 인자에 중점을 두었습니다.
인슐린 유사 성장 인자 1(IGF1)의 증가와 IGF 결합 단백질 3(IGFBP3)의 감소가 종양 형성 및 전이와 관련되어 있다는 점을 감안할 때 한 연구에서는 레스베라트롤 보충제((0.5, 1.0, 2.5, and 5 g/day for 29 days; n =10–12/dose)의 이러한 단백질의 순환 수준에 대한 효과를 조사했습니다..
보충 29일 후, 저자들은 하루 2.5g의 레스베라트롤 치료가 혈장 내 IGF1 및 IGFBP3 수치를 유의하게 감소시켰으며, 이는 인간에서 화학 예방제로 레스베라트롤의 사용을 뒷받침할 수 있음을 발견했습니다.
1.0g/day 용량은 또한 치료 전 기준 수준과 비교하여 혈장 IGFBP3의 상당한 감소를 야기했습니다.
두 가지 더 높은 용량은 여러 피험자에게 단기적으로 경증에서 중등도의 위장 증상을 유발했습니다( Brown et al . 2010 ).
다른 시험에서는 건강한 피험자에게 4주 동안 1g의 레스베라트롤을 투여하고 림프구 수치 또는 발암 및 약물 대사에 관여하는 효소의 활성 수치를 나타내는 대리 지표를 측정했습니다( Chow et al . 2010).
레스베라트롤 보충제는 글루타티온 S- 트랜스퍼라제 및 글루쿠로노실 트랜스퍼라제와 같은 다양한 발암 물질 해독 효소의 단백질 또는 활성 수준을 증가시켰지만, 기준선에서 효소 수준이 낮은 경우에만 상당한 증가에 도달했습니다.
Chow et al . (2010) 은 약리학적 레스베라트롤 보충제가 잘 견디는 것처럼 보이고 발암물질의 해독 강화를 통해 암 보호 효과를 발휘할 수 있지만 사이토크롬 P450의 억제를 통해 다양한 약물의 대사를 변경할 가능성이 있을 수도 있다는 중요한 경고를 언급했습니다. .
따라서 레스베라트롤의 안전성과 이점은 특히 약제와 함께 투여하는 맥락에서 더욱 자세히 설명되어야 합니다.
이 제한된 임상 시험 데이터에서 레스베라트롤이 암 예방 또는 치료를 위한 실행 가능한 옵션으로 간주되기 전에 훨씬 더 많은 인간 연구가 필요하다는 것이 분명합니다.
재발성 또는 불응성 다발성 골수종 환자를 대상으로 한 2상 임상 시험에서 레스베라트롤 5g/일 용량은 부작용(메스꺼움, 설사, 피로 및 신장 독성 포함)을 유발하여 한 환자의 사망과 조사관이 연구를 조기에 종료하게 했습니다( Popat et al . 2013).
저자는 이 고용량이 건강한 환자를 대상으로 한 다른 임상 시험에서 안전한 것으로 나타났습니다.
이것은 생체 내 암 모델 에서 레스베라트롤의 효능과 안전성에 대한 더 많은 연구의 필요성을 강조합니다 .
경구 투여 후, 트랜스 -레스베라트롤은 글루쿠로니드와 황산염으로 빠르게 접합됩니다.
경구 투여 후 트랜스 -레스베라트롤 의 생체이용률 이 낮기 때문에, 연구자들은 최근 생체이용률이 더 높은 레스베라트롤 유도체의 효과를 조사하기 시작했습니다(.
후추에서 발견되는 화합물인 피페린은 글루쿠론산화를 억제할 수 있습니다.
생쥐에서 피페린은 두 화합물의 경구 투여 후 레스베라트롤의 혈청 수준을 유의하게 증가시켰습니다.
다른 연구에서는 암 모델에 대한 레스베라트롤 및 멜라토닌, 차 폴리페놀 및 케르세틴과 같은 기타 자연 발생 화합물의 시너지 효과에 초점을 맞추었습니다. 이러한 연구에 대한 철저한 검토는 Singh et al 참조. (2013)..
레스베라트롤은 비만 동물 모델과 고지방식이에 많은 긍정적인 영향을 미치는 것으로 나타났기 때문에 암 예방 분야에서 고려해야 할 중요한 분자입니다.
레스베라트롤 치료는 또한 식이 유발 당뇨병 모델에서 고혈당증을 감소시켰을 뿐만 아니라 증가된 지방량으로 인해 인슐린 저항성이 발생했을 때 인슐린 감수성을 개선했습니다.
일부 초기 임상 시험에서 레스베라트롤 보충제는 내당능 장애가 있는 노인 대상의 포도당 조절을 개선하고 비만 남성의 항상성 모델 평가 지수를 개선했습니다.
또한 제2형 당뇨병 환자의 레스베라트롤 보충제를 조사한 두 개의 개별 연구에서 레스베라트롤은 인슐린 감수성과 HbA1c 측정을 개선했습니다.
다른 그룹은 레스베라트롤 치료로 인슐린 감수성 또는 포도당 조절의 개선을 보여줄 수 없었습니다.
정상 체중과 비만 대상 모두에서 레스베라트롤 사용은 고인슐린혈증-정상혈당 클램프로 측정했을 때 조직으로의 인슐린 감수성과 포도당 흡수를 개선할 수 없었습니다.
**********************************************************************************
'약물' 카테고리의 다른 글
| DIM이란 ? I3C와 동일한가? (0) | 2022.10.26 |
|---|---|
| Matrine-간암 (0) | 2022.10.26 |
| 비타민 C 약동학: 경구 및 정맥내 사용에 대한 의미 (0) | 2022.10.17 |
| 암에 대한 비타민 C 경구복용 테스트 (0) | 2022.10.16 |
| 식이 폴리페놀 및 이들의 생물의약품 분류 시스템 (0) | 2022.10.10 |